DOI: 10.20986/resed.2021.3855/2020
ARTÍCULO
OPIOIDES EN LA ARTROSIS
OPIOIDS IN OSTEOARTHRITIS
J. Tornero Molina1
1Servicio de Reumatología. Hospital General Universitario de Guadalajara. Departamento de Medicina y Especialidades Médicas. Universidad de Alcalá de Henares. Madrid, España
ABSTRACT
Osteoarthritis (OA) rank highly among global causes of disability and chronic pain. OA is also responsible for substantial health and societal costs, both directly and as a consequence of impaired work productivity and early retirement. Despite numerous efforts, treatments to paliate the impact of the disease have not reached a threshold of efficacy. We review the utility of opioids for the treatment of pain due to OA. Opioids provide no clinically relevant pain relief in the short- and intermediate-term for osteoarthritis pain. They provide a clinically relevant reduction in disability in the short but not in the intermediate term. The short- and intermediate-term tolerability of opioids is low. Therefore, opioids have a limited role in the management of OA pain in selected patients.
Key words: Osteoarthritis, opioids, pain
RESUMEN
La artrosis (OA) es una de las principales causas de discapacidad y dolor crónico. La OA es también responsable de un sustancial coste sociosanitario, tanto directo como por la pérdida de productividad laboral e invalidez. A pesar de numerosos esfuerzos, los tratamientos para mitigar el impacto de esta enfermedad no han alcanzado el umbral deseable de eficacia. Revisamos la utilidad de los opioides para la terapia del dolor de la OA. Los opioides proporcionan un alivio clínicamente poco relevante del dolor en el corto y medio plazo. Pueden mejorar la capacidad funcional a corto, pero no a medio plazo. La tolerabilidad a estos agentes es baja. Por lo tanto, los opioides juegan un papel limitado en el manejo del dolor por la OA en un reducido grupo de pacientes.
Palabras clave: Artrosis, opioides, dolor
Correspondencia: Jesús Tornero Molina
jtorneromolina@ser.es
INTRODUCCIÓN
La artrosis es una enfermedad articular caracterizada por degeneración y pérdida del cartílago hialino articular y el fibrocartílago de meniscos y discos intervertebrales, junto con cambios reactivos en el hueso subcondral, proliferación ósea marginal, fibrosis capsular y episodios intercurrentes de sinovitis. La artrosis es la artropatía más frecuente en el adulto y una de las enfermedades con mayor prevalencia en la raza humana (1). El estudio EPISER 2016 (2,3) estableció que la artrosis sintomática afecta al 29,35 % de la población adulta española; la artrosis de cadera al 5,13 %, la de manos al 7,73 %, la de rodilla al 13,83 % y la de columna lumbar al 15,52 %.
La artrosis produce dolor, discapacidad, pérdida de jornadas laborales y de ingresos económicos, así como un gran sufrimiento físico y psíquico a las personas que la padecen (4,5,6,7). En ausencia de tratamiento médico curativo, el objetivo que se persigue es el alivio sintomático del proceso, algo desgraciadamente no siempre fácil de conseguir. Existen numerosas guías de práctica clínica para el tratamiento de las artrosis desarrolladas por organizaciones científicas. Entre ellas se incluyen las del American College of Rheumatology y la Arthritis Foundation (8), la de la European League Against Rheumatism (9,10), de la Osteoarthritis Research Society International (11), y la del National Institute for Health and Care Excellence (12).
Sin embargo, a pesar de toda la información y consejos incluidos en las mismas, con base en la evidencia científica y la opinión de expertos, es importante reseñar que desgraciadamente el efecto global y los resultados obtenidos con la aplicación de estas distan mucho de ser satisfactorios. Menos del 50 % de los pacientes con artrosis reúnen criterios de cuidado óptimo, cifra inferior a la de otras condiciones crónicas como la diabetes o la osteoporosis (13). Los dominios en los que el cuidado de la artrosis es peor incluyen el tratamiento farmacológico y no farmacológico, con una idoneidad de tan solo el 40 %.
Los fármacos opioides forman parte de la escalera analgésica de la OMS (diseñada inicialmente para el dolor oncológico), siendo introducidos como tratamiento del dolor crónico no maligno en la década de los años 80 del siglo pasado. A raíz de esto, en los últimos 30 años, el mundo ha presenciado un aumento progresivo en el consumo de estos fármacos. Entre los años 1985 y 1994, el consumo de opioides en España se multiplicó por 10; la dosis diaria definida por millón de habitantes pasó de ser 94,7 a 1023,9 (14). Entre 2007 y 2014, el 17 % de los sujetos con artrosis de EE. UU. recibía opioides (15); en 2014 el 30 % de las prescripciones a largo plazo de opioides en Alemania se dirigían al tratamiento sintomático de la artrosis (16).
No obstante, hoy en día existe una gran controversia sobre la verdadera utilidad de los opioides en el tratamiento prolongado del dolor crónico no oncológico, como es el de la artrosis (17). De esta manera asistimos a la así conocida como “epidemia de opioides” o “crisis de los opioides”. Consiste esta en la detección, en EE. UU., de un incremento en la prescripción de estos agentes terapéuticos con abuso de los mismos. Todo esto hace necesario clarificar cuál es el verdadero papel y beneficio que aportan los fármacos opioides al tratamiento del dolor por artrosis (18).
El objetivo de esta revisión narrativa es aclarar la eficacia y seguridad de los fármacos opioides en la terapia de la artrosis, en base a la literatura existente, con el fin último de demostrar si realmente tienen utilidad clínica. Dicho beneficio clínico debe ser valorado en contraposición al riesgo de padecer sus efectos adversos y, en concreto, al riesgo de desarrollar adicción a los mismos. Así, se podrá conocer el peso que deben tener realmente estos fármacos en la práctica clínica.
EFICACIA DE LOS OPIOIDES EN EL DOLOR POR ARTROSIS
Una revisión sistemática (RS) y metanálisis (MA) reciente ha evaluado la eficacia, tolerabilidad y seguridad de los opioides comparándola con placebo, en el dolor crónico por la artrosis (19). Los autores realizaron una búsqueda sistemática en Clinicaltrials.gov, Central, Medline y PsycINFO desde octubre de 2013 hasta julio de 2019. Se incluyeron ensayos clínicos aleatorizados que compararan opioides con placebo, de al menos cuatro semanas de observación. Las variables primarias de desenlace analizadas fueron: alivio del dolor igual o mayor del 50 %, discapacidad, tolerabilidad y seguridad. La estimación del efecto de cada intervención se evaluó: a) para las variables continuas mediante diferencia estandarizada de las medias (con intervalos de confianza al 95 %) y b) para las variables dicotómicas, a través de la diferencia de riesgos. Para clasificar el tamaño del efecto se considera (en una diferencia estandarizada de las medias) que este es pequeño cuando es 0,2, mediano si es mayor de 0,2 y menor de 0,5 y grande cuando ronda el valor de 0,8.
Se revisaron un total de 22 estudios con 8942 sujetos incluidos. Ocho estudios evaluaron la oxicodona, seis trabajos el tramadol; se recogieron dos estudios para cada uno de los siguientes fármacos: buprenorfina, hidromorfona, morfina y tapentadol. Finalmente hubo un estudio de codeína, fentanilo y oximorfona para el análisis. La mayoría de los ensayos utilizaron preparaciones de liberación retardada de los opioides; un estudio empleó morfina de liberación rápida. Los pacientes incluidos presentaban artrosis de cadera y/o rodilla. En 17 estudios se excluyeron sujetos con antecedentes de trastornos mentales y abuso actual o pasado de drogas. La calidad de los estudios analizados es baja o muy baja.
Utilizando métodos de imputación, los autores concluyen que los opioides no aportan beneficios significativos frente a placebo en orden a la reducción igual o mayor de un 50 % del dolor por artrosis. Se detecta una reducción clínicamente relevante de la discapacidad a corto plazo, pero no en los estudios con seguimiento intermedio o prolongado. Tampoco se considera relevante la proporción de pacientes que reducen la intensidad media de su dolor o que refieren encontrarse mejor o mucho mejor con el tratamiento con opioides. Frente a placebo no se detecta diferencia en la aparición de acontecimientos adversos graves, aunque la tolerabilidad de los opioides es peor.
Dos estudios de tapentadol (20,21), incluidos en esta RS y MA, en artrosis de rodilla y/dolor lumbar crónico encuentran, frente a placebo, una reducción media de la intensidad del dolor de 0,56 unidades (IC 95 %: 0,20 a 0,92) con un riesgo incrementado de abandono por efectos adversos de 1,36 (IC 95 %: 1,13 a 1,64) (22).
Solo 2 de los 22 estudios analizados investigaron la existencia previa de conductas sospechosas de abuso de drogas y no encontraron hallazgos de adicción en opioides de prescripción (19). Sin embargo, los mismos autores se sorprenden de la escasa monitorización sistemática previa del riesgo de adicción, cuando el peligro de abuso con estos fármacos era conocido en EE. UU. desde el año 2000 (23).
Bialas y cols. han realizado otra RS y MA para evaluar la eficacia, aceptabilidad y seguridad del tratamiento a largo plazo con opioides en el dolor crónico no maligno, incluyendo la artrosis (24). Interrogaron a las bases de datos (Clinicaltrials.gov, central y Medline) hasta junio de 2019, analizando las extensiones abiertas de duración igual o superior a 26 semanas de ensayos clínicos previos con una duración igual o superior a 2 semanas. Estudiaron los datos continuos con la diferencia estandarizada de las medias y los categóricos con tasas de frecuencia. Recogieron información de 15 estudios con 3590 participantes. La duración de los estudios oscilaba entre 26 y 156 semanas y su calidad era muy baja. Los individuos analizados padecían artrosis, dolor lumbar y dolor neuropático. Solo el 31,1 % de los sujetos randomizados basalmente terminaron el periodo de observación abierto. La diferencia estandarizada de las medias para el cambio en la intensidad del dolor entre el final del periodo doble-ciego y el final del periodo de la extensión abierta fue de 0,06 (-0,03, 0,15) y para la función física de -0,12 (-0,24, 0,00). El 14,1 % de los pacientes abandonaban el tratamiento por efectos adversos; en el 6,3 % se trataba de acontecimientos adversos graves. Se detectó utilización inadecuada y conducta aberrante hacia el opioide en el 2,7 % de los casos.
Los autores concluyen que en el contexto de estos estudios de extensión abierta los opioides mantienen su eficacia de reducción del dolor y la discapacidad, aunque la tasa de supervivencia de los tratamientos es baja. Se podría, por ello, en la opinión de este grupo de investigación, considerar (para pacientes que en tratamientos a corto plazo hubieran experimentado mejoría) prolongar a largo plazo la terapia con estos agentes terapéuticos. Sin embargo, esto exigiría una minuciosa selección de los casos y una monitorización y seguimiento estrechos.
Sicras-Mainar y cols. (25) estudiaron la carga de la enfermedad y sus costes en pacientes con dolor moderada a severa por artrosis, refractario al tratamiento convencional, en el sistema nacional de salud español. Realizaron un estudio longitudinal retrospectivo, de práctica real, no intervencionista. Incluyeron pacientes de edad igual o superior a 18 años con dolor crónico moderado-severo por artrosis que no respondía a los cuidados estándar con fármacos antinflamatorios no esteroideos (AINE) combinados con opioides. La carga de la enfermedad se evaluó midiendo la analgesia, la función cognitiva, las actividades básicas de la vida diaria, la gravedad y la frecuencia de las comorbilidades y la mortalidad por cualquier causa. Se determinaron los costes por la utilización de los cuidados sanitarios y los relacionados (precios de 2018).
Se analizaron 13.317 casos, con una edad media de 68,9 años. El 71,3 % eran mujeres; el 58,1 % no habían respondido a AINE con opioides débiles y el 41,9 % eran refractarios a la combinación de AINE + opioides fuertes. La media de comorbilidades fue de 2,9. El dolor disminuyó en 0,9 puntos y la función cognitiva en 2,2 puntos; la dependencia empeoró en 0,4 puntos a lo largo de un periodo de tratamiento de 188,6 días tratados con AINE seguidos por 400,6 días en los que recibieron opioides. La tasa de mortalidad ajustada fue mayor en los pacientes con artrosis que tomaban AINE + opioides fuertes (hazard ratio: 1,44, 1,26-1,63, p < 0,001). El coste a 4 años de los cuidados de salud fue de 7350 euros por paciente y fue más alto en aquellos que tomaron opioides fuertes frente a los que recibieron opioides débiles (9886 € vs. 5519 €, p < 0,001). El coste de la analgesia (16 % del coste total, 70, 2% por opioides) fue mayor con los opioides fuertes que con los débiles (19,6 % vs. 11,3 %, p < 0,001).
Los autores concluyen que, en la práctica clínica habitual en España, los pacientes con dolor crónico moderado a severo por artrosis rebelde al tratamiento estándar con AINE + opioides describen reducciones muy modestas en la intensidad del dolor, mientras que presentan una considerable carga de comorbilidades, deterior cognitivo y nivel de dependencia. Los costes sanitarios se ven incrementados significativamente para el sistema nacional de salud, especialmente por la combinación de fármacos antinflamatorios no esteroideos (AINE) y opioides.
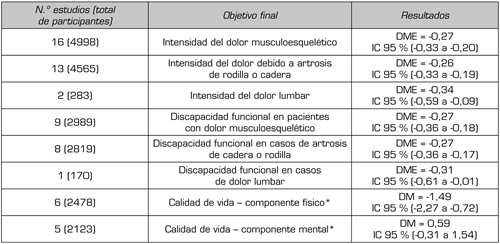
Megale y cols. (26) han estudiado también, mediante MA, la eficacia de los opioides para reducir la intensidad del dolor y para mejorar la capacidad funcional de los pacientes con dolor musculoesquelético, buscando la asociación de estas variables con la dosis diaria empleada y con la duración del tratamiento. Las Tablas I y II exponen sus principales resultados. Los autores concluyen que, en la población analizada (edad media = 60 años) los analgésicos opioides tienen un efecto pequeño en la disminución de la intensidad del dolor (diferencia estandarizada de medias = -0,27; IC 95 % = -0,33 a -0,20) y en la mejoría de la capacidad funcional (diferencia estandarizada de las medias = -0,27, IC 95 % = -0,36 a -0,18). Este efecto no se relaciona con la dosis diaria ni con la duración del tratamiento. La probabilidad de presentar acontecimientos adversos es tres veces mayor con los opioides (odds ratio = 2,94, IC 95 % = 2,33-3,72); la probabilidad de interrupción del tratamiento es cuatro veces mayor también con estos últimos analgésicos (odds ratio = 4,04, IC 95 % = 3,10-5,25). Estos resultados sugieren que en pacientes ancianos con dolor musculoesquelético el tratamiento con analgésicos opioides tiene solo un efecto leve sobre el dolor y la función, a costa de un mayor riesgo de presentar efectos adversos y discontinuación del tratamiento.
Tabla I. Eficacia de opioides frente a placebo. Tamaño del efecto

DM: diferencia de medias. DME: diferencia de medias estandarizada. IC: intervalo de confianza.
Tabla II. Asociación de la eficacia de los opioides con la dosis diaria y con la duración
del tratamiento (*)
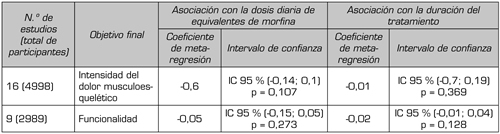
*Análisis de metaregresión, donde la correlación es menor cuanto más cercano a 0 sea el coeficiente y es mayor cuanto más cercano a 1. Con valores negativos se considera que la relación entre las variables estudiadas es inversa, mientras que será directa si se obtiene un valor positivo.
Modificado de referencia bibliográfica 26.
Un asunto importante para aclarar en el tratamiento de la artrosis es la eficacia comparada que presentan, en el alivio del dolor, diferentes grupos de analgésicos. Un metanálisis (27) realizó una metaregresión para estudiar las diferencias estadísticamente significativas entre diferentes tipos de fármacos a la hora de reducir la intensidad del dolor, basándose en 17 estudios. Los fármacos comparados fueron opioides leves (tramadol, tramadol-paracetamol), opioides fuertes (hidromorfona, oxicodona) y AINE (celecoxib, diclofenaco, naproxeno, piroxicam). Los resultados mostraron la inexistencia de diferencias clínicamente relevantes o estadísticamente significativas entre los tres grupos de fármacos (p = 0,22). Sin embargo, se observó que los pacientes con niveles medios de dolor mayores, según el cuestionario WOMAC, respondieron con más cambios en la intensidad del dolor, siendo estos resultados estadísticamente significativos (p < 0,001). Del mismo modo, la reducción del dolor fue mayor en pacientes con artrosis de rodilla frente a los que la presentaban en la cadera (p < 0,01).
Finalmente, Schaefert y cols. (28) revisaron mediante metanálisis 16 estudios, con un total de 6743 participantes; demostraron con significación estadística la superioridad de los opioides frente a placebo en la reducción del dolor crónico no tumoral, con los siguientes estadísticos: DME = -0,22, IC 95 % (-0,28; -0,17); p < 0,00001; I2 = 21 %; calidad de la evidencia moderada. Sin embargo, no hubo superioridad en la reducción del 50 % del dolor. Por otro lado, sí que detectaron superioridad frente a placebo en causar fuertes mejorías del estado general de los pacientes (p = 0,002) y en la mejoría de su capacidad funcional física (p < 0,00001), siendo discutible el tamaño del efecto en este último caso.
Hasta la fecha no tenemos disponible ningún ensayo clínico randomizado (ECR) en el que se hayan realizado comparaciones directas (“head to head”) y son escasa también las RS y MA en red que evalúen en paralelo todas las opciones farmacológicas disponibles para el tratamiento del dolor en la artrosis. Una RS ya mencionada que incluyó ECR de al menos 8 semanas de duración con fármacos AINE (27 ramas de tratamiento) y opioides (14 ramas de tratamiento) encontró que los AINE y los opioides presentaban una eficacia similar en el alivio del dolor (27). Un estudio pragmático randomizado (29) de 12 meses, realizado en sujetos con lumbalgia crónica o artrosis de cadera o rodilla, no encontró ventajas significativas en la escalada a la terapia con opioides (estadio 1: morfina, hidrocodona/paracetamol, oxicodona liberación inmediata; estadio 2: morfina y oxicodona de liberación sostenida; estadio 3: fentanilo transdérmico) comparándola con una escalada terapéutica con medicación no opioide (estadio 1: paracetamol, AINE; estadio 2: medicación oral adyuvante y analgésicos tópicos; estadio 3: pregabalina, duloxetina, tramadol). Estas dos estrategias terapéuticas exhibían efectos similares en la reducción del dolor y la discapacidad, en la tolerabilidad y en la seguridad (incluyendo el potencial de abuso).
TOLERABILIDAD Y SEGURIDAD DE LOS OPIOIDES EN LA ARTROSIS
El MA de Smith y cols. (27) no detectó diferencias significativas entre opioides y placebo en cuanto a la aparición de acontecimientos adversos (AA) graves. Recogió 7 estudios (4694 participantes) en los que se analizaron los casos mortales secundarios al tratamiento. En el grupo experimental falleció un paciente de 2752, frente a 4 fallecidos de 1942 en el grupo control, por lo que la reducción del riesgo fue de 0,00 (IC 95 % [-0,00; 0,00]; p = 0,88; I2 = 0 %; calidad de la evidencia moderada).
Respecto a la tolerabilidad del tratamiento opioide frente a placebo, el MA ya citado de Schaefert (28) encontró que la tasa de abandono debida AA en el grupo tratado con opioides fue mayor que en el grupo control (p < 0,00001), resultando un NNH de 5 (IC 95 %4-6). Tampoco se demostró una diferencia significativa entre la aparición AA graves o eventos mortales entre el grupo control y el experimental.
La Tabla III expone los resultados obtenidos en cuanto a efectos adversos y abandono del tratamiento en el metanálisis de Megale (26). Se considera, en la actualidad, que un 8 % de los pacientes con dolor crónico desarrollan adicción a los opioides, mientras que un 15-26 % participa del abuso o el mal uso de estos fármacos (30). Además, el 82 % de las muertes secundarias a sobredosis de opioides son accidentales o se relacionan con un uso inapropiado (17,31). El abuso de opioides prescritos se relaciona también con la existencia concomitante de depresión o ansiedad. Aparece también relación causal con la tendencia a la catastrofización del dolor. La incidencia de abuso de estos fármacos se ve aumentada con la prescripción de opioides de liberación rápida en comparación con aquellos de liberación prolongada (26).
Tabla III. Tolerabilidad y seguridad de los opioides

IC: intervalo de confianza. Nº: número. OR: odds ratio frente al comparador/placebo.
Kostev y cols. (32) evaluaron la persistencia de la terapia con opioides en una gran cohorte de pacientes (n = 32,158) con dolor crónico no maligno. Al cabo de 1 año de seguimiento el 69 % había abandonado la medicación. La probabilidad de interrupción de la terapia se relacionaba con a la enfermedad, la edad, y las comorbilidades y la depresión. Shcherbakova y cols. (33) estudiaron de forma retrospectiva una cohorte de 302 pacientes que iniciaron tratamiento con buprenorfina/naloxona para dolor crónico; y encontraron una adherencia del 40,4 % por año de seguimiento. La adherencia al tratamiento se incrementaba con la educación y la información del paciente; los pacientes más adherentes tenían menos ingresos hospitalarios (34).
CONSIDERACIONES FINALES
Muchos estudios analizados se han realizado en centros de investigación. Son pocos los estudios, incluidos en estas RS y MA, desarrollados en el ámbito de la medicina de atención primaria (básicamente son estudios abiertos que no se incluyen en muchas de estas publicaciones analizadas previamente). En muchos ensayos clínicos se excluyen pacientes con patología orgánica mayor, edad avanzada y trastornos mentales. Sin embargo, la artrosis afecta a muchas de estas poblaciones.
Los estudios realizados se focalizan generalmente en artrosis de cadera o rodilla, probablemente porque son modelos clínicos de dolor artrósico poco contaminados, más fáciles de evaluar. Sería bueno ampliar el conocimiento a localizaciones también frecuentes de la artrosis como son los dedos de las manos, la acromioclavicular o la trapecio-metacarpiana del pulgar.
Algunos estudios no describen claramente características de los pacientes tan importantes como la duración de los síntomas y el uso de medidas complementarias de tratamiento (fundamentalmente medidas físicas). Los resultados sobre la función articular se representan en forma de diferencia de medias, sin hacer una clara referencia a los cambios clínicamente relevantes.
Solo unos pocos trabajos analizan el efecto sobre el sueño, la dependencia física o la adicción. Finalmente, la mayoría de los estudios incluidos en estas RS y MA de ensayos clínicos no permiten obtener conclusiones de la eficacia y seguridad a largo plazo (más de 6 meses); se necesita complementar la información con la procedente de extensiones abiertas de los mismo, tal y como recomienda la Agencia Europea del Medicamento.
Los AINE y los opioides pueden proporcionar discretas reducciones del dolor y mejorar la capacidad funcional en los pacientes con artrosis, pero con un margen de tolerabilidad y seguridad que puede llegar a ser comprometido. Como ya hemos comentado anteriormente, Smith y cols. (27) encontraron que los AINE y los opioides ejercían un efecto similar sobre el alivio del dolor en la artrosis. Fuggle y cols. (35) recuerdan que existen problemas de seguridad y tolerabilidad en el uso de opioides para el tratamiento de la artrosis y defienden las recomendaciones internacionales que aconsejan su uso por periodos cortos de tiempo y después del fallo de otros analgésicos. Esta pauta y recomendación terapéutica puede proporcionar al paciente un grado aceptable de analgesia, sin afectar a la función cognitiva o las actividades básicas de la vida diaria.
Indicaciones potenciales para el uso de opioides en la artrosis podrían incluir: a) dolor severo y convincente, asociado a daño orgánico demostrable y avanzado; b) dolor severo refractario a otros tratamientos no farmacológicos y farmacológicos, en pacientes con y sin artroplastia; c) pacientes con contraindicaciones absolutas para el uso de fármacos AINE y/o reemplazamiento protésico articular; d) uso intermitente durante cortos periodos de tiempo para tratar crisis dolorosas intercurrentes. En estos casos, si se considerase indicada la terapia con opioides se utilizarán las dosis recomendadas por las guías más recientes sobre el uso prolongado de opioides en el dolor crónico no maligno. Según estas recomendaciones, el rango de dosis debería estar entre 90 (36,37) y 150 mg/día de morfina (36,37,38) o el equivalente para otro opioide. Al igual que con cualquier tratamiento la terapia con opioides, solo se debe mantener si existe un beneficio clínico con la misma (reducción significativa del dolor y/o de la discapacidad) y el perfil de tolerabilidad/seguridad del tratamiento son aceptables (39).
La última actualización de la Guía OARSI de tratamiento de la artrosis no recomienda el uso de opioides orales o transdérmicos en individuos con artrosis, debido a las alarmas internacionales recientemente emitidas por el riesgo de dependencia química asociada a estas medicaciones (11,40,41). Este rechazo se fundamenta además en la evidencia de que su eficacia sobre los síntomas de la artrosis es limitada o irrelevante (27,29,42).
CONCLUSIONES
La utilidad de los opioides fuertes en el alivio del dolor por cáncer está demostrada; sin embargo, es controvertida su eficacia en la mitigación del dolor no debido a neoplasia. Existen dudas sobre su utilidad a largo plazo y los efectos sobre la recuperación funcional en pacientes con artrosis, cuando se comparan con otros analgésicos. Los opioides presentan efectos adversos que pueden conducir a la suspensión del tratamiento por intolerancia; también pueden desencadenar dependencia en un porcentaje de casos. Por lo tanto, ante un sujeto con dolor por artrosis lo recomendable es individualizar su terapia analgésica adaptándola al tipo de pacientes y a la clase de dolor, evaluando reglada y sistemáticamente los beneficios y riesgos del tratamiento.
BIBLIOGRAFÍA