ORIGINAL
10.20986/resed.2024.4089/2023
Bloqueo brilma guiado por ultrasonido para manejo del síndrome doloroso postmastectomía en pacientes oncológicos: una serie de casos
Ultrasound guided brilma block for the management of post-mastectomy pain syndrome in oncological parients: a series of cases
Jessica Román Romero1
Edith Aguilar Galindo2
Irais Cordova González3
1Servicio de Clínica del Dolor y Cuidados Paliativos. Unidad de Oncología de los Servicios de Salud del Estado de Puebla, México
2Servicio de Anestesiología. Hospital Universitario de Puebla, México
3Servicio de Clínica del Dolor. Hospital General de Puebla, México
RESUMEN
Introducción: El síndrome doloroso postmastectomía se define como el dolor persistente que aparece poco después de la mastectomía/lumpectomía, y cuya prevalencia es alrededor del 20-60 % de los pacientes sometidos a mastectomía; en cuanto a las características del dolor se describe de tipo neuropático. Por otra parte, el bloqueo modificado de las ramas intercostales laterales a nivel medio axilar se postula como una alternativa para el manejo analgésico de este síndrome doloroso el cual es considerado como una técnica mínimamente invasiva, de baja dificultad de ejecución.
Objetivo: Determinar la disminución de dolor en pacientes con síndrome doloroso postmastectomía después del bloqueo BRILMA guiado por ultrasonido.
Pacientes y métodos: Previo a aceptación del procedimiento, colocación del paciente y bajo técnica estéril, se procedió a realizar el bloqueo BRILMA ecoguiado, una vez identificadas las estructuras anatómicas de acuerdo con la técnica descrita, se colocó aguja en el plano interfascial y se administró un volumen total de 15 cc compuesto por (5 cc ropivacaÍna 0,187 % + 2 cc dexametasona de depósito 4 mg + 8 cc de agua inyectable).
Resultados: Se incluyeron un total de 6 mujeres con síndrome doloroso postmastectomía, sometidas a bloqueo BRILMA durante julio a diciembre de 2022, en la Unidad de Oncología. Se encontró una disminución del dolor mayor al 50 % sobre la intensidad basal. La duración de la disminución del dolor por encima del 50 % posterior al procedimiento fue de 4-8 meses. Se disminuyeron las dosis de fármacos y, por lo tanto, efectos indeseables.
Conclusión: Pese a la limitación que existe en la literatura por no contar con reportes de estudios grandes que implementen la técnica realizada en este estudio, para el manejo del síndrome doloroso postmastectomía, se encuentra descrito que los abordajes interfaciales son una opción factible. Los procedimientos intervencionistas presentan múltiples beneficios, por lo que es importante continuar con las líneas de investigación para poder encontrar mejores alternativas en el tratamiento del dolor.
Palabras clave: Dolor crónico postmastectomía, bloqueo nervios intercostales, bloqueo Brilma, técnicas intervencionistas, ultrasonografía
ABSTRACT
Introducción: Post-mastectomy pain syndrome is defined as persistent pain that appears shortly after mastectomy/lumpectomy, and the prevalence is about 20-60 % of patients undergoing mastectomy, as for the characteristics of pain is described as neuropathic. On the other hand the modified block of the lateral intercostal branches at the middle axillary level, it is postulated as an alternative for the analgesic management of this pain syndrome which is considered a minimally invasive technique and low difficulty of execution.
Objective: Determine decrease of pain in patients with post-mastectomy pain syndrome after ultrasound-guided BRILMA block.
Methods: Prior to acceptance of the procedure, placement patient, and sterile technique; the ultrasound-guided BRILMA Block was performed, once the anatomical structures were identified according?to the technique described, the needle was placed in the interfacial plane and to manage a volume of 15?cc?which is composed of (5 cc ropivacaine 0.187 % + 2 cc dexamethasone depot 4 mg + 8 cc of water for injection) was administered.
Results: A total of 6 women with post-mastectomy pain syndrome were included for the Brilma block during July to December 2022, of the Oncology Unit. A decrease in pain was found to be greater than 50% over the basal intensity. The duration of pain decrease above 50% after the procedure was 4 to 8 months. The drug doses and therefore undesirable effects were decreased.
Conclusion: Despite the limitation that exist in the literature for not having reports of large studies that implement the technique carried out in this study, for the management of postmastectomy pain syndrome, it is described that interfacial approach are a feasible option. Interventional procedures have a multiple benefits, so it´s important to continue with the lines or research in order to find better alternatives in the treatment of pain.
Key words: Chronic postmastectomy pain, intercostal nerve block, brilma block, interventional techniques, ultrasonography.
Correspondencia
Jessica Román Romero
dra.jessicaroman@gmail.com
Recibido: 29-06-2023
Aceptado: 12-11-2024
Román Romero J, Aguilar Galindo E, Cordova González I. Bloqueo Brilma guiado por ultrasonido para manejo del síndrome doloroso postmastectomía en pacientes oncológicos: una serie de casos. Rev Soc Esp Dolor. 2024;31(2):85-0
INTRODUCCIÓN
El cáncer de mama representa el 11,7 % de todos los casos de cáncer en el año 2020 (1). A pesar de su elevada prevalencia, solo representa el 6,9 % de las muertes relacionadas con el cáncer en el mundo, en gran parte debido a las innovaciones en el cribado, secuenciación genética y modalidades de tratamiento dirigido (2). Las pacientes que han sido diagnosticadas con cáncer de mama son tratadas quirúrgicamente con diversas formas de mastectomía, cirugía conservadora de la mama y disección de ganglios linfáticos que, con frecuencia, dan lugar a la formación de dolor crónico (1).
La Asociación Internacional para el Estudio del Dolor (IASP) define el síndrome doloroso postmastectomía (SDPM) como el dolor persistente que aparece después de la mastectomía/tumorectomía, afectando la parte anterior del tórax, axila y/o la parte superior y medial del brazo. En general, la IASP establece 3 meses como límite para considerar un dolor como crónico. Sin embargo, prefiere a menudo el periodo de 6 meses para fines de investigación (3).
Se estima que el SDPM varía dependiendo de la bibliografía consultada sin embargo, ocurre en alrededor del 20 % al 60 % de los pacientes sometidos a mastectomía (4). Perdura por un periodo igual o mayor a 3 meses posterior a la mastectomía, e incluso puede presentarse hasta 10 años postcirugía (4).
Walto y Rockwell describen el síndrome de dolor postmastectomía como un dolor que se produce después de cualquier cirugía de mama; de al menos intensidad moderada, se localiza en la mama, región torácica, axila o brazo ipsilateral, con una duracion mínima de 6 meses, ocurriendo al menos en el 50 % del tiempo, y puede ser exacerbado por los movimientos de la cintura escapular (5). Presenta características neuropáticas que a menudo es descrito por los pacientes como ardor, sensaciones dolorosas de frío o descargas eléctricas, así como entumecimiento, hormigueo o sensaciones de alfileres y agujas (6). Es probablemente secundario a una lesión del nervio intercostobraquial o intercostales durante la disección a nivel axilar, lo que explica las características neuropáticas de este dolor (7).
Existen múltiples opciones de tratamiento farmacológico y/o no farmacológico que han sido propuestas por asociaciones internacionales, las cuales postulan como primera línea de tratamiento fármacos como antidepresivos tricíclicos, inhibidores de la recaptura de serotonina y noradrenalina, inhibidores selectivos de la recaptrua de serotonina o gabapentinoides (1). La respuesta al tratamiento farmacológico para el dolor neuropático se percibe de manera individual, variada e impredecible; por tal motivo se debe encontrar el fármaco/combinación de fármacos y/o técnicas de intervención que sean bien tolerados, con la menor cantidad de efectos secundarios posibles y, por lo tanto, resulte en el adecuado control del dolor para el paciente (8).
El bloqueo de las ramas cutáneas de los nervios intercostales en la línea medio axilar (BRILMA) fue descrito por primera vez en 2012 por Fajardo y cols.?(9). Recordando un poco de anatomía, tenemos que el nervio intercostal realiza su división en ramos cutáneos anteriores y laterales, los cuales se producen a nivel de la línea media axilar, y que son los responsables de la inervación de la glándula mamaria. Por lo tanto, el objetivo del bloqueo BRILMA es colocar el transductor en la línea medio axilar e inyectar anestésico local entre el músculo serrato anterior y los músculos intercostales externos, permitiendo el bloqueo del ramo cutáneo lateral y del nervio intercostal, previamente a su división en ramo anterior y posterior y, además existe un bloqueo también del ramo cutáneo anterior del nervio intercostal por difusión del anestésico desde los músculos intercostales externos a los íntimos. Esta difusión se observó en estudios en cadáveres; observando como el azul de metileno llega incluso al pulmón, debido a que los músculos intercostales se comportan como un entramado muscular muy poroso fácilmente evidenciable en disección cadavérica (10).
Su aplicación como técnica anestésica en cirugía no reconstructiva de mama ha demostrado un manejo del dolor en estos pacientes efectivo; además, se propone como una técnica fácil de ejecutar, reproducible en la mayoría de los pacientes, y segura para realizarse aún fuera del área quirúrgica (9) como también se plasma en este trabajo.
Yango y cols. (11) realizaron una propuesta de algoritmo de manejo intervencionista para los pacientes con dolor postcirugía de mama en donde, dependiendo de la localización del dolor, se puede optar por distintos abordajes. Entre las opciones descritas se encuentra el bloqueo del plano profundo del músculo serrato, que en su técnica es muy parecido al bloqueo BRILMA, y los pacientes sometidos a este procedimiento se reportan con adecuado control del dolor, se plasman como recomendaciones para su aplicación, el utilizar un volumen de 10 ml de una combinacion de anestésico local y esteroide de depósito. El bloqueo del músculo serrato se propone como una opción en el manejo de los pacientes con síndrome doloroso postmastectomía, en pequeñas series de casos, como la publicada por Zocc y cols. (12). De igual manera lo reportan Liu y Khanna (13) en su trabajo de investigación, donde se propone el uso de las ténicas guiadas por ultrasonido, tanto en planos superficiales como profundos del músculo serrato, siendo buenas opciones de manejo en casos de dolor persistente con características neuropáticas y que se distribuye en zonas axilar y/o anterolateral de la región pectoral. Dicho método de infiltración en su técnica es muy similar al propuesto en este trabajo; en cuanto a reproducibilidad y seguridad es una opción factible con buena eficacia; sin embargo, al igual que el bloquo BRLMA, no existen publicaciones con tamaños de muestras grandes. Existen algunos trabajos, como el de Baytar y cols. (14), donde se compara su uso versus la aplicación de infiltraciones paravertebrales, en donde se han obtenido resultados similares en cuanto mejoría del dolor y reducción en el uso de opioides. Sin embargo, las infiltraciones de ramos superficiales son opciones seguras y más rápidas en su realización. Chang y cols. (15), en su revisión sobre enfoques específicos, mencionan la utilidad de este tipo de abordajes para el tratamiento de dolor con una distribución más amplia. Si bien, en la revisión de la literatura no se pudieron encontar estudios grandes con la implementación de esta técnica en específico para el manejo del dolor crónico, podemos mencionar sin lugar a dudas que las técnicas intervencionistas tienen cada vez un lugar más importante en el manejo del dolor, con múltiples beneficios que como profesionales de la salud ya conocemos; este punto nos motiva a seguir las líneas de investigación para poder encontrar mejores alternativas en el tratamiento del dolor.
La Clínica del Dolor en donde se tratan estos pacientes pertenece al sistema de salud público, por lo que continuamente nos enfrentamos a escasez de insumos; además, la población atendida en la mayoría de los casos, no posee el recurso económico para adquirir de manera constante analgésicos en caso de reportarse fármacos faltantes, por lo que las autoras continuamente se encuentran en la búsqueda de optimizar los recursos existentes, tratando de obtener la mejor propuesta de manejo para asegurar un mejor control del dolor en nuestros pacientes, y por lo tanto se vea reflejado en la calidad de vida de nuestra población.
Esta serie de casos es la primera en examinar la eficacia de bloqueo BRILMA para el tratamiento de síndrome doloroso postmastectomía.
METODOLOGÍA
Hipótesis
El bloqueo BRILMA es un tratamiento efectivo para manejo del dolor en pacientes con diagnóstico de síndrome doloroso postmastectomía.
Se trata de un estudio retrospectivo, longitudinal, experimental, en el cual se identificaron las pacientes con diagnóstico de síndrome doloroso postmastectomía con mala respuesta a tratamiento farmacológico, específicamente por una inadecuada tolerancia a los efectos adversos de dichos fármacos. Previo a autorización por el comité de ética institucional, se procedió a realizar el estudio bajo la invitación y aceptación de los pacientes en participar, tanto para el estudio y uso de datos recabados en anonimato, como para la intervención.
Los pacientes que conformaron el estudio, se sometieron al procedimiento bloqueo interfascial BRILMA durante el periodo julio a diciembre de 2022, en la Unidad de Oncología de los Servicios de Salud del Estado de Puebla. Se incluyeron un total de 6 pacientes con diagnóstico de SDPM, con síntomas como parestesias, disestesias, dolor tipo punzante y ardoroso, así como alodinia, como principales presentaciones clínicas.
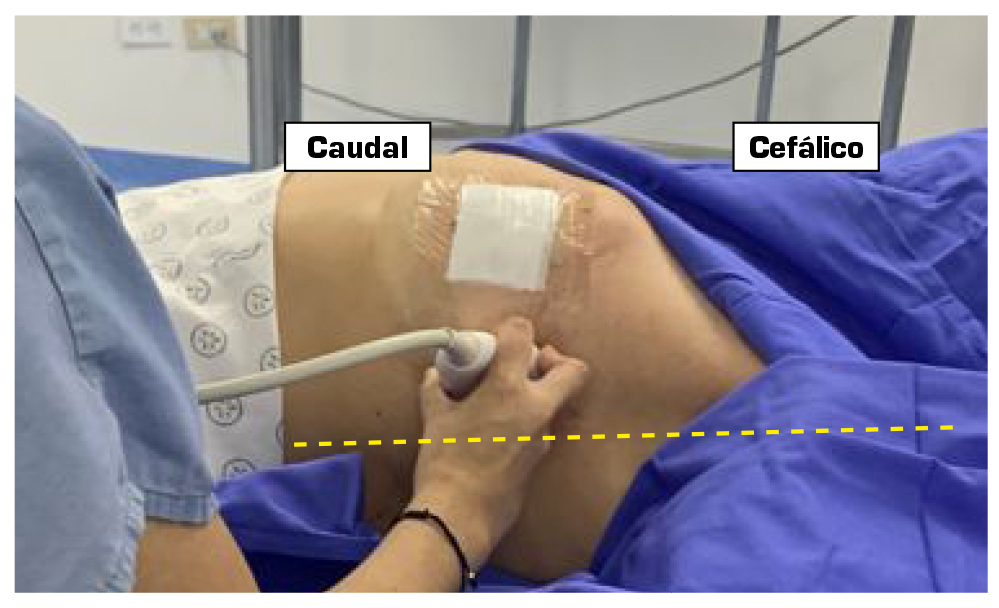
Todos los paciente con presencia del SDPM, que no tuvieran alguna contraindicación para el procedimiento, se les propuso la realización de un bloqueo BRILMA como opción para el control del dolor. Los riesgos y beneficios se discutieron con el paciente antes del procedimiento y de aceptarse se firmó un consentimiento informado para su realización. Los procedimientos se llevaron a cabo en una sala quirúrgica, bajo monitorización estándar y con manejo anestésico de sedación superficial. Los pacientes fueron colocados en decúbito lateral con la región afectada hacia arriba, o en decúbito prono con la región afectada hacia el operador. Después de la preparación estéril, se utilizó una sonda de ultrasonido lineal colocándose en el eje longitudinal de la pared torácica lateral a nivel de la linea axilar media (Figura 1).

Figura 1. Colocación de transductor en la línea media axilar.
Se identificaron las siguientes imágenes ecográficas: en el plano superficial se identifica el tejido celular subcutáneo, en el plano intermedio el músculo dorsal ancho, el músculo serrato anterior (SAM), las costillas (C) y?entre estas los músculos intercostales (externo, interno e?íntimo) y en plano profundo pleura y pulmón (Figura 2).
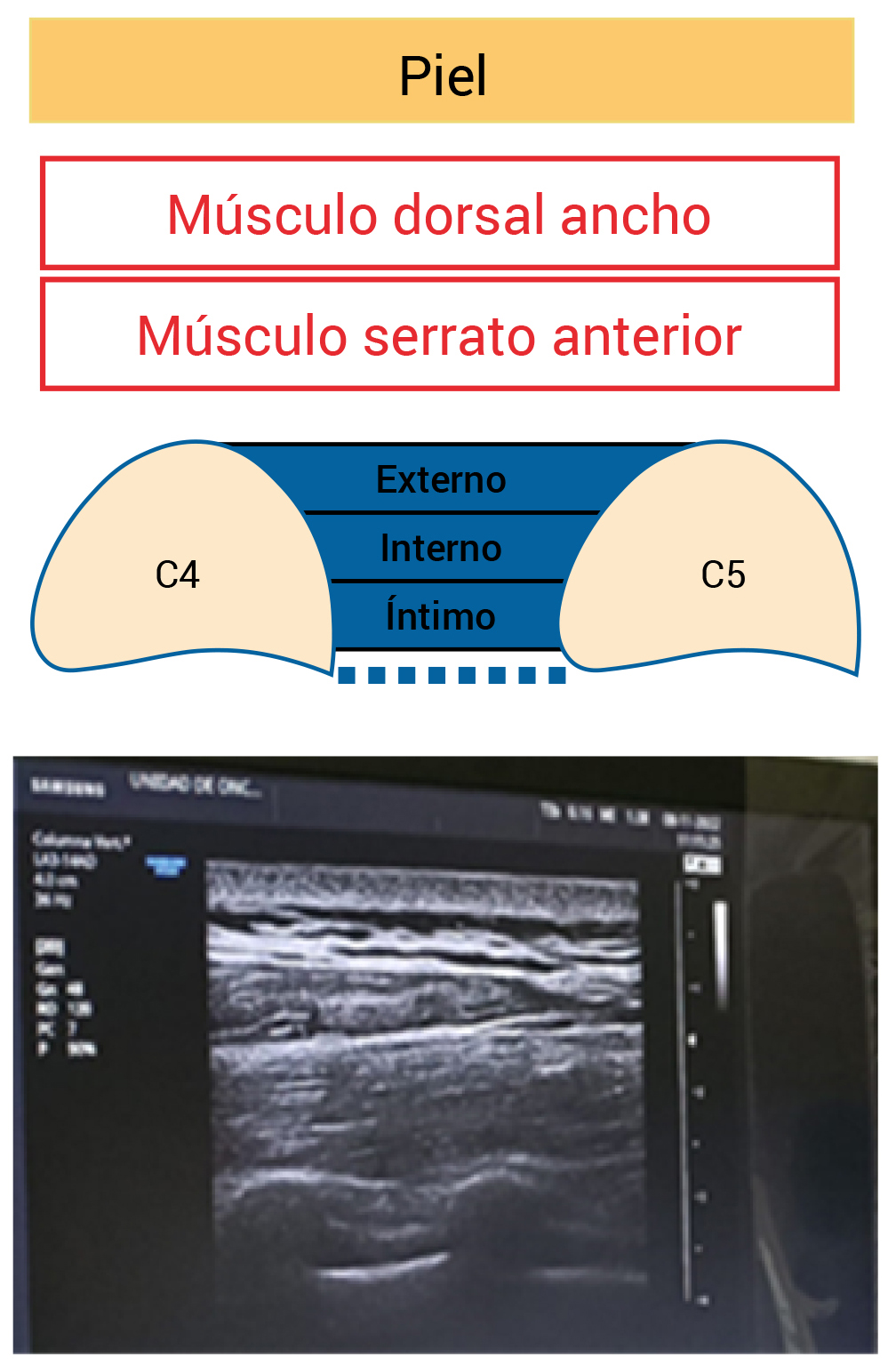
Figura 2. Identificación de las estructuras ecográficas.
El abordaje se realizó en plano, introduciendo una aguja ecogénica de 100 mm por el borde inferior de la sonda en dirección de caudal a craneal, avanzando cuidadosamente sin dejar de ver la punta de la aguja hasta posicionarla entre el músculo serrato anterior y el músculo intercostal externo. Se comprobó la correcta posición de la punta de la aguja administrándose una dosis test de 1 ml de lidocaína al 1 %, observando la distensión del plano interfascial y posteriormente se inyectaron 3 ml por segmento (Figura 3). El volumen total utilizado fue de 15 ml compuesto por (5 ml ropivacaína 0,187 % + 2 ml dexametasona de depósito 4?mg + 8 ml de suero fisiológico).
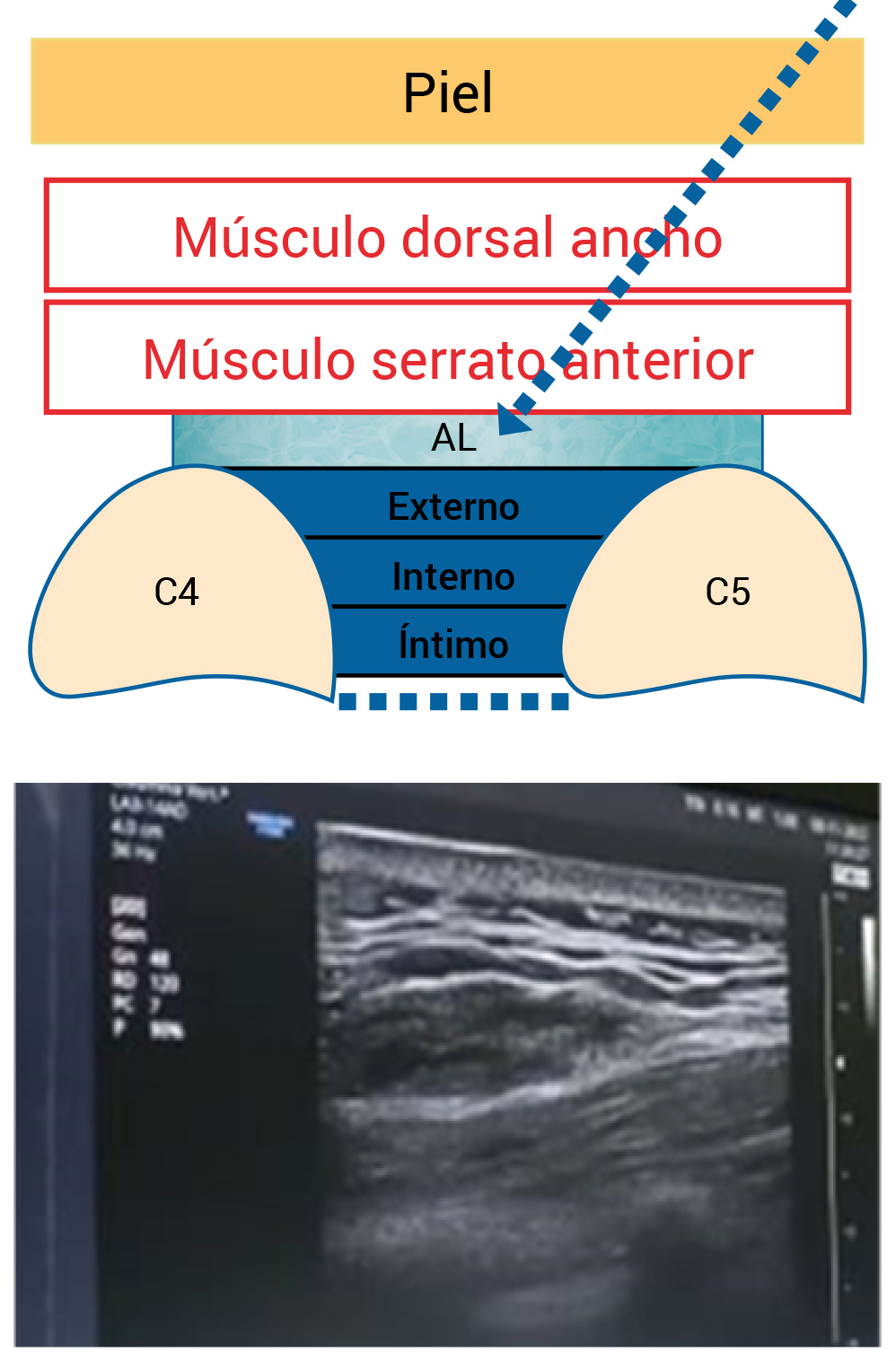
Figura 3. Identificación de las estructuras ecográficas e hidrodisección con anestésico local.
Al finalizar el procedimiento y corroborar que no existió alguna eventualidad relacionada con el mismo, las pacientes fueron egresadas de la unidad de cuidados postanestésicos y citadas a la consulta externa de clínica del dolor en la primer semana postprocedimiento para su evaluación, utilizando la escala verbal numérica, la cual se registró en su expediente, así como cualquier modificación en sus tratamientos analgésicos farmacológicos, y los efectos adversos de los mismos si existía, cada mes para continuar seguimiento, obteniendo un alcance de hasta 8 meses.
RESULTADOS
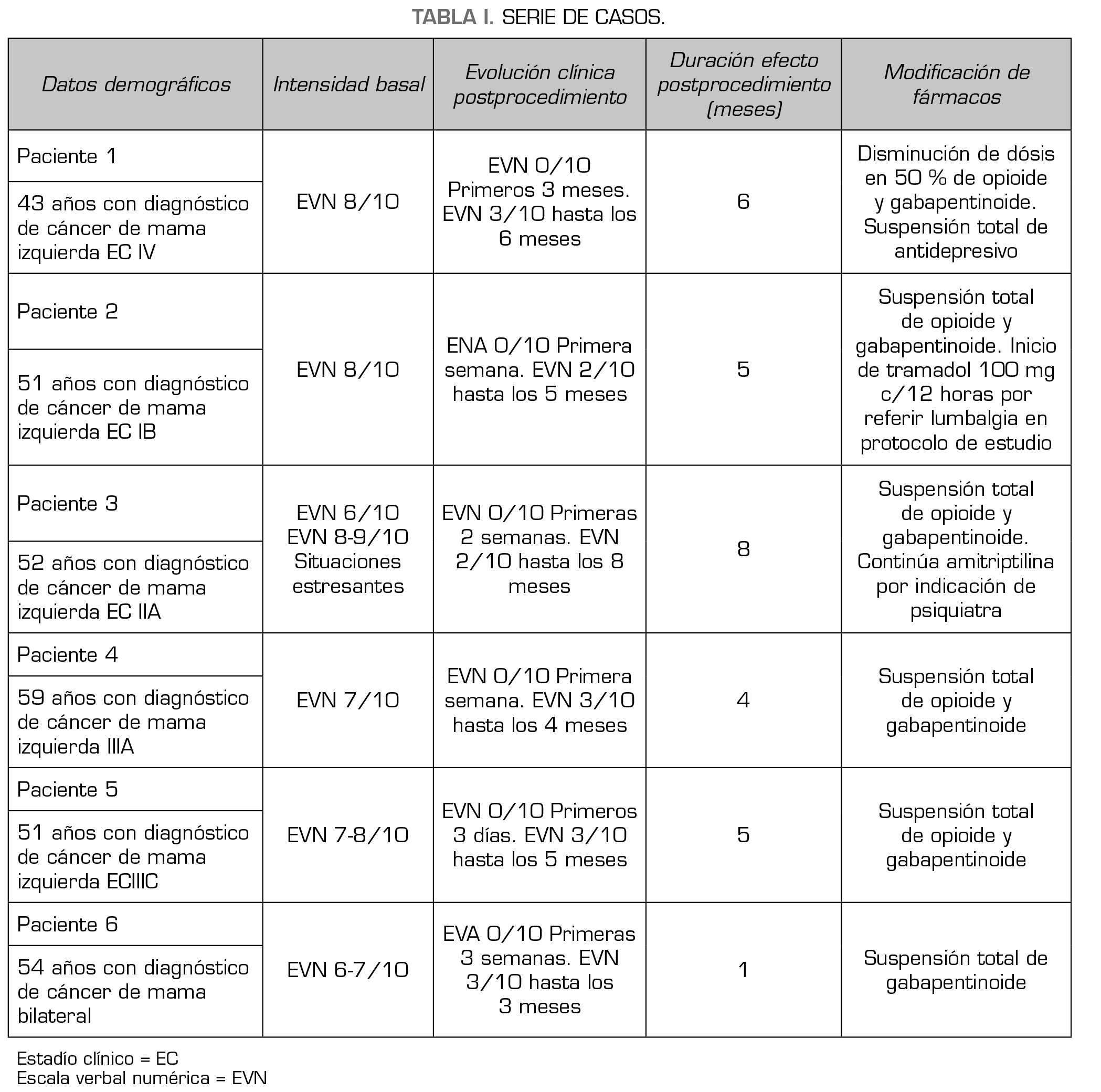
Todos los pacientes fueron de género femenino en un rango de edad de 40-50 años. Las 6 mujeres sometidas al procedimiento experimentaron una disminución del dolor mayor al 50 % tomando en cuenta la intensidad basal, para su evaluación se utilizó la escala verbal numérica. La duración de la disminución del dolor por encima del 50 % del dolor basal posterior al procedimiento fue de 4-8 meses. Además se disminuyeron las dósis de fármacos y por lo tanto la presencia de efectos indeseables (Tabla 1).
DISCUSIÓN
Se presenta una serie de casos de un grupo de pacientes con antecedente de cáncer de la glándula mamaria postoperados de mastectomía en algunos casos en combinación con esquemas de quimioterapia y radioterapia, así como terapia hormonal. Las pacientes desarrollaron síndrome doloroso postmastectomía y fueron atendidas en la clínica del dolor, implementando de manera inicial tratamiento farmacológico utilizando distintas combinaciones de opioides, gabapentinoides y antidepresivos conforme a las guías de manejo para esta patología (16); a las pacientes a las que se les propuso tratamiento intervencionista fueron aquellas con mala tolerancia a efectos adversos o con poca mejoría del dolor a pesar de tratamiento farmacológico; las candidatas al procedimiento fueron sometidas a la realización de un bloqueo tipo BRILMA guiado por ecografía, en la clínica del dolor de la Unidad de Oncología de los Servicios de Salud del estado de Puebla.
Este estudio tiene la limitación de ser una pequeña series de casos; sin embargo, la eficacia que se logró con el bloqueo en las 6 pacientes tuvo un buen periodo de duración, comprendiendo que solo se realizó como técnica analgésica/desinflamatoria y se evidenció, además, la disminción de uso de fármacos o de dosis; por lo tanto la presencia de efectos adversos, así como mejoría en la calidad de vida de las pacientes, merece más investigación en este campo.
Como se señaló anteriormente, las opciones de tratamiento para pacientes con SDPM incluyen tratamiento médico, bloqueos nerviosos y ablación nerviosa, sin embargo, ninguna de estas modalidades ha demostrado proporcionar un alivio constante del dolor (17). Dentro de la bibliografía podemos encontrar un estudio realizado por Elsayed y cols., (18) en el cual realizan un bloqueo de nervios con anestásico local y lo complementan con ablación por radiofrecuencia para el tratamiento de neuralgia intercostal resistente, teniendo como resultados una mejoría del dolor durante más de 1 año, por lo cual se puede considerar en un futuro implementar estas dos técnicas para el control del dolor por un periodo más prolongado.
CONCLUSIONES
El manejo del dolor crónico en pacientes que experimentan SDPM es complejo; por lo tanto, las autoras de este trabajo postulan que el bloqueo de los nervios intercostales en el espacio serratointercostal (bloqueo BRILMA) es una alternativa terapéutica eficaz para los pacientes que experimentan dolor crónico postquirúrgico, ya sea por mala tolerancia a efectos adversos de la terapia farmacológica, o por no tener un control del dolor eficaz a pesar de tener esquema de analgesia multimodal. Esta alternativa es una técnica de baja dificultad de ejecución, con una econatomía fácil de comprender, reproducible en la mayoría de los pacientes, el cual puede ser realizado de manera segura, además con mínimas complicaciones y con una alta tasa de éxitos, como se reportó en los casos expuestos.
CONFLICTO DE INTERESES
Los autores declaran no tener ningún conflicto de intereses.
FINANCIACIÓN
Ninguna.
BIBLIOGRAFÍA