10.20986/resed.2025.4128/2024
REVISIÓN
Dolor de miembro fantasma. Comprensión y abordaje terapéutico más allá de la terapia en espejo
Phantom limb pain. Understanding and therapeutic approach beyond mirror therapy
Natalia Botero Jaramillo1
Iván Mauricio González Zambrano2
1Médica, antropóloga, magíster en historia y residente de medicina del dolor y cuidados paliativos. Universidad de La Sabana e Instituto Nacional de Cancerología. Colombia
2Médico, especialista en medicina física y rehabilitación, docente y especialista de la Clínica Universidad de La Sabana. Colombia
RESUMEN
El dolor de miembro fantasma se define como un tipo de dolor neuropático. Sin embargo, tiene unas características propias por los cambios corticales que se producen posterior a una amputación y la sensación fantasma que involucra. La presente revisión de la literatura ofrece una síntesis de las teorías fisiopatológicas de dicha entidad, su presentación y evaluación clínica. Por último, explora las distintas estrategias de tratamiento tanto no farmacológico como farmacológico, ofreciendo información sobre la utilidad de las técnicas y su relación con la fisiopatología de la enfermedad, así como los resultados de los estudios, principalmente de los ensayos clínicos y de las revisiones sistemáticas y metaanálisis, para exponer las mejores opciones terapéuticas.
Palabras clave: Dolor de miembro fantasma, dolor neuropático, amputación, tratamiento, rehabilitación
ABSTRACT
The phantom limb pain is defined as a kind of neuropathic pain, however, it has its own characteristics due to the cortical changes that occur after an amputation and the phantom limb sensation that involves. The present review of the literature offers a synthesis of the pathophysiological theories, its presentation and clinical evaluation. Finally, explore the different treatment strategies both non -pharmacological and pharmacological, offering information on the usefulness of techniques and their relationship with the disease, as well as the results of the studies, mainly of the clinical trials and the systematic reviews and meta -analysis, to expose the best therapeutic options.
Key words: Phantom limb pain, neuropathic pain, amputation, treatment, rehabilitation
Correspondencia:
Natalia Botero Jaramillo
nboteroj@gmail.com
Recibido: 16-01-2024
Aceptado: 28-06-2024
INTRODUCCIÓN Y APROXIMACIÓN HISTÓRICA
El dolor de miembro fantasma (DMF) es una entidad poco comprendida, pese a sus casi cinco siglos de historia. Se diferencia de la sensación de miembro fantasma al ser una experiencia que causa dolor y sufrimiento. Es importante tener presente que este fenómeno se presenta solo en los adultos, siendo un evento menos frecuente en los niños, y esto, debido a los fenómenos corticales que explican su etiopatología (1,2). El DMF se define como la percepción de dolor o molestia en una extremidad que ya no está allí (3). Este fenómeno fue reconocido por primera vez por el cirujano francés del renacimiento Ambroise Paré en 1551, quien habría practicado abundantes amputaciones a soldados; sin embargo, el término específico de miembro fantasma se atribuye a Silas Weir Mitchell, quien en 1872 publicó un estudio sobre amputaciones traumáticas de la guerra civil de Estados Unidos (3).
Después de una amputación se pueden presentar al menos dos tipos de dolor, uno es el dolor residual de la extremidad y el otro el DMF. Para diferenciar el dolor residual de la extremidad del DMF se debe tener en cuenta la localización del dolor, y el tiempo de inicio y curso del mismo. El dolor residual tiene una noxa identificada y se produce en el muñón cuando hay atrapamiento de nervio, desarrollo de un neuroma, un trauma quirúrgico (3) o por prótesis mal ajustadas (Prostógena) (4). Por el contrario, el DMF proviene de la parte amputada del cuerpo y no hay una causa única identificable, se puede presentar en compañía de dolor residual, y permanece durante más tiempo, usualmente se presenta al mes de la amputación, y tiene una pobre respuesta a los tratamientos por lo que se tiende a cronificar (4). Este se describe como un dolor de tipo neuropático, puede presentarse no solo ante la amputación de una extremidad, sino también en otras partes amputadas como los senos, el pene, los testículos, el útero, los ojos, la lengua o incluso un diente (5).
Los principales factores asociados al desarrollo de esta entidad fueron analizados por Limakatso y cols. en un metanálisis a partir de 15 estudios, con 4102 pacientes, identificando al menos 25 factores (6) y siendo los principales factores de riesgo con alta evidencia y una fuerte asociación el dolor de la extremidad residual, el dolor previo a la amputación y las sensaciones fantasmas no dolorosas (7). El objetivo de este artículo de revisión literaria es ofrecer una síntesis de las teorías fisiopatológicas del DMF, su presentación, evaluación clínica y las distintas estrategias de tratamiento tanto no farmacológico como farmacológico, ofreciendo información sobre la utilidad de las técnicas y su relación con la fisiopatología de la enfermedad.
METODOLOGÍA
La presente revisión tiene como propósito hacer una revisión narrativa teniendo presente los criterios de la Scale for Assessment of Narrative Review Articles (SANRA), con el objetivo de actualizar el conocimiento sobre el DMF en su fisiopatología, el abordaje clínico y los tratamientos tanto farmacológicos como no farmacológicos, incluyendo aquellos que se proponen desde la medicina física y de rehabilitación, y que integran la terapia física y la terapia ocupacional, así como los avances en psicología. Se privilegiaron las técnicas ampliamente difundidas, y algunas que por su innovación están marcando nuevos paradigmas en su manejo, tales como la terapia en espejo (TE) acompañándola de estimulación nerviosa, las técnicas que integran realidad virtual, la imaginería motora, y las técnicas desde la psicología. Se realizó una búsqueda en las principales bases de datos (PubMed y Lilacs) con los términos MESH en español y en inglés de “phantom limb” and “pain” and “treatment” and “rehabilitation”, y “dolor de miembro fantasma”, “tratamiento”, “rehabilitación”, y se hizo una selección de artículos no sistemática, por conveniencia, se llevo a cabo una lectura crítica de la literatura, y se revisó por cada tema y técnica la evidencia realizando una exposición de los principales resultados de los estudios, así como de los consensos científicos sobre el tema. Se incluyeron aquellos artículos que hablaran directamente del fenómeno desde una perspectiva médica, y que abordaran diversos métodos de tratamiento. Se tomaron como apoyo algunas revisiones de la literatura previas a este artículo para complementar las teorías fisiopatológicas, así como revisiones sistemáticas y metaanálisis, y en el apartado de tratamiento se tomaron estudios clínicos aleatorizados, y estudios observacionales para evaluar la efectividad de las intervenciones de manera descriptiva. Se encontró un total de 206 artículos.
RESULTADOS
En EE. UU. al año se realizan 30.000 a 40.000 amputaciones, y en total hay 1,6 millones de amputados (3). El DMF ocurre en un 60-85 % de los adultos amputados, siendo la enfermedad vascular periférica la principal causa (1). El DMF se puede presentar hasta en un 50 % en las primeras 24 horas posterior a la amputación y en un 85 % en la primera semana, y se manifiesta un segundo pico a los 12 meses postamputación. El estudio de Kooijman y cols. encontró una relación entre el DMF y la sensación fantasma de un 67 % con un riesgo relativo de 11,3; es decir que se presenta al menos 11 veces más cuando se tiene sensación fantasma, y el dolor fantasma con el dolor residual de la extremidad tiene un riesgo relativo de 1,9 (8). La incidencia más baja calculada a un mes fue de 2,2 %, a los 3 meses aumenta a un 41 % y a los 12 meses hasta un 82,7 % (2).
FISIOPATOLOGÍA
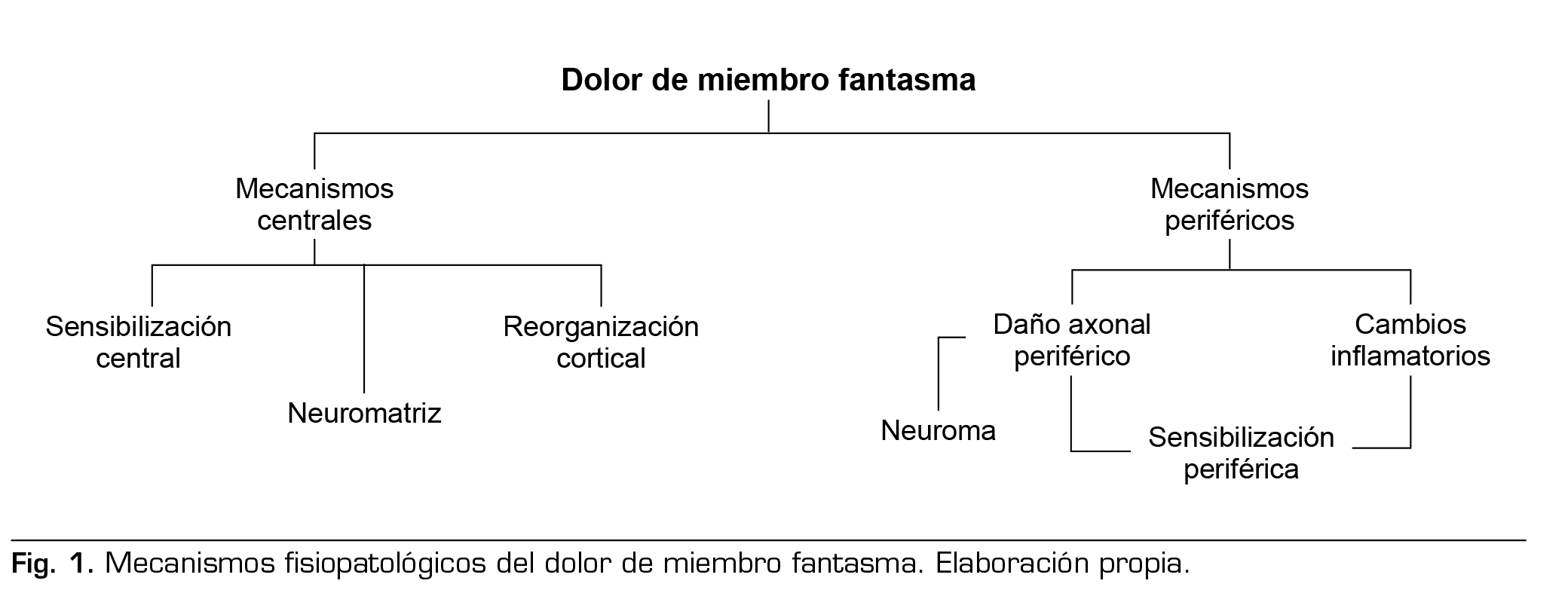
La fisiopatología del DMF no está completamente esclarecida, lo que impacta en su abordaje terapéutico, ya que sus mecanismos no se comprenden en su totalidad y existen múltiples teorías que intentan explicar la complejidad del fenómeno (Figura 1) (9). Una de las teorías más estables en el tiempo es la irritación de las terminaciones nerviosas amputadas; sin embargo, en los últimos años se ha demostrado la importancia del sistema nervioso central para explicar el establecimiento del DMF, mediante las teorías de la neuromatriz, la reorganización cortical, la sensibilización central y la memoria propioceptiva (3,10,11).

MECANISMOS PERIFÉRICOS
A nivel periférico, la amputación significa una pérdida de continuidad, que genera terminales nerviosas cortadas. Estas neuronas se tornan hiperexcitables, lo que se explica por un incremento en los canales de sodio, con descargas espontáneas y aumento de transmisiones nociceptivas a la médula espinal, con descargas anormales en la asta dorsal (5). El proceso de amputar genera además cambios inflamatorios y la formación de neuromas, que se explican por mecanismos de brote y crecimiento neuronal desordenado, con actividad patológica. Se observan conexiones no funcionales entre los axones, lo que contribuye a disparos nerviosos anormales, que pueden ser desencadenados por algunos estímulos como la presión generada por las prótesis, y los cambios de temperatura extremos. Las descargas ectópicas se dan tanto por fibras A-Beta como por fibras C (1,3,4). Los neuromas no son condición necesaria para provocar el DMF y más bien definen el dolor residual, sin embargo, el dolor el dolor residual de extremidades se relaciona con un mayor desarrollo de DMF (12). Otro de los fenómenos de transformación con el DMF es la transformación del cuerpo del ganglio de la raíz dorsal, con un aumento en la excitabilidad posterior a la transección axonal, que involucra mecanismos de respuesta inflamatoria, que incluyen quemoquinas, interleuquinas, factor de necrosis tumoral, y que forman parte de los fenómenos de sensibilización periférica (4,13).
MECANISMOS CENTRALES
Se han descrito al menos tres mecanismos centrales que son la teoría de la reorganización cortical, la teoría de la sensibilización de la médula espinal y la teoría de la neuromatriz. La primera teoría de la reorganización cortical consiste en que las áreas corticales que representan la extremidad u órgano amputado las asumen las áreas de representación vecinas en la corteza somatosensorial y en la motora (5,14). Estos cambios se han podido observar en la electroencefalografía, magnetoencefalografía, resonancia magnética funcional o estimulación magnética transcraneal, haciendo una caracterización de la somatotopía, es decir las áreas de representación cortical tanto motoras como sensoriales. En estos estudios, los pacientes con miembros amputados mostraron una superposición de la zona de desaferenciación cortical con regiones cerebrales vecinas en la corteza somatosensorial y motora, siendo este proceso de reorganización cortical propio de los pacientes con DMF (10,15). Esto no ocurre de forma inmediata sino cuando se cronifica el dolor, permitiendo la consolidación del DMF, mediante la plasticidad cerebral y la reorganización cortical, así como la efectividad de las terapias que apuntan a procesos cognitivos como la terapia en espejo (TE) (10,14). Este fenómeno no se limita a la corteza, sino que también se ha visto en el tálamo y sus circuitos neuronales (4,14).
A nivel de la médula espinal, se da un proceso de sensibilización central, por el aumento de la actividad del NMDA en la asta dorsal de la médula espinal, haciéndola más sensible a la sustancia P, taquiquininas y neurocinas, seguida de una regulación ascendente de los receptores en dicha área, y esto contribuye a la alodinia e hiperalgesia. Se altera la función de las interneuronas GABAérgicas y glicinérgicas inhibitorias (3,15,16). El sistema simpático también contribuye mediante el acoplamiento de neuronas sensitivas y simpáticas y un aumento de norepinefrina postsinápitca, la cual se relaciona con hiperalgesia y aumento de nocicepción espinal. Adicionalmente se ha descrito una regulación a la baja de los receptores opioides luego de un daño nervioso importante como ocurre en la amputación, produciéndose un aumento de la colecistoquinina en el dolor crónico, que es un inhibidor endógeno de los receptores de opioides, lo que genera más dolor en el tejido lesionado (1).
La teoría de la neuromatriz propuesta por Melzack propone una red de neuronas en varias áreas del cerebro (incluye el tálamo, la corteza somatosensorial, formación reticular, sistema límbico, corteza parietal posterior, que no solo son áreas nociceptivas) que responden a los estímulos sensoriales y producen patrones específicos de impulsos llamados “neurofirma”, los cuales si bien se activan por entradas sensitivas, no son dependientes de estas, por lo que se pueden mantener pese a la ausencia de estímulos. Esto registra que el cuerpo está intacto, por lo que cuando se presenta la amputación la ausencia de estas señales crea una neurofirma anormal que genera el DMF (5,11,14). Por tanto, cuando se amputa una extremidad se genera un cortocircuito en que no se envían señales sensitivas de la extremidad ausente, lo que genera un cambio mal adaptativo en la neuromatriz que lleva a patrones internos de dolor y localización en la extremidad amputada (11).
La memoria propioceptiva es otro fenómeno en el que el paciente con DMF siente la extremidad amputada, e incluso percibe su posición y movimiento con actos volitivos. Otro fenómeno propioceptivo tiene que ver con la posición en la que es amputada la extremidad, que recuerda previa a la anestesia, y que informa al paciente en relación con la sensación y el dolor. O con otros recuerdos de posiciones dolorosas en el pasado que se reviven con el DMF. Por tanto, desencadenar ese recuerdo doloroso hará que el sujeto ponga fin al mismo, al realizar una retroalimentación propioceptiva y visual que le permita re-acomodar la extremidad a una postura no dolorosa. Esta teoría explica tanto la importancia de la posición en que se amputó la extremidad, como la utilidad de la TE y de realidad virtual que se explicarán más adelante (4,14).
PRESENTACIÓN CLÍNICA
Según la Clasificación Internacional de Enfermedades CIE-11, el DMF está clasificado como un trastorno de dolor neuropático (17), cuyo dolor puede ser típicamente neuropático en su origen y está referido al miembro amputado con sensaciones de tipo corrientazo, pinchazo, quemantes o palpitante (18). Sin embargo, como advierten Schone y cols., es que existe una gran heterogeneidad en las sensaciones, clasificadas como no dolorosas y dolorosas, que superan la sola definición de dolor neuropático (7). En algunos casos se siente la extremidad amputada como congelada. En otros casos, resulta doloroso para el paciente imaginar que se mueve la extremidad, o experimentan la sensación de movimiento involuntarios como espasmos, o sensación de que se empuña (19). También se puede dar el fenómeno llamado “telescoping”, que es la sensación de acortamiento de la extremidad fantasma, la cual es de buen pronóstico y está presente en algunos procesos de resolución del dolor (20).
El paciente puede presentar hormigueo, palpitaciones, sensación de punción por agujas en la extremidad inexistente. Se debe hacer una historia clínica y un examen físico completo a fin de descartar otros diagnósticos diferenciales. Se aconseja examinar la piel, las articulaciones por encima de la amputación, y se pueden usar algunas ayudas paraclínicas para descartar causas subyacentes, por ejemplo, un hemograma y reactantes de fase aguda para infección, una ecografía para neuromas, una valoración psicológica para aquellos pacientes con un alto componente emocional del dolor, estrés postraumático, ansiedad o depresión (3). Aunque no existe una escala específica para la valoración del dolor por miembro fantasma, la literatura recomienda algunos instrumentos de dolor neuropático que pueden ser útiles al ser el DMF de dichas características. Para diagnosticar un dolor neuropático, se requiere al menos la existencia de una lesión nerviosa o enfermedad, y una distribución de síntomas neuroanatómicamente plausible, además con una cercanía temporal entre el daño y la aparición de los síntomas, y la confirmación de sensaciones negativas o positivas clásicas del dolor neuropático (16,20,21).
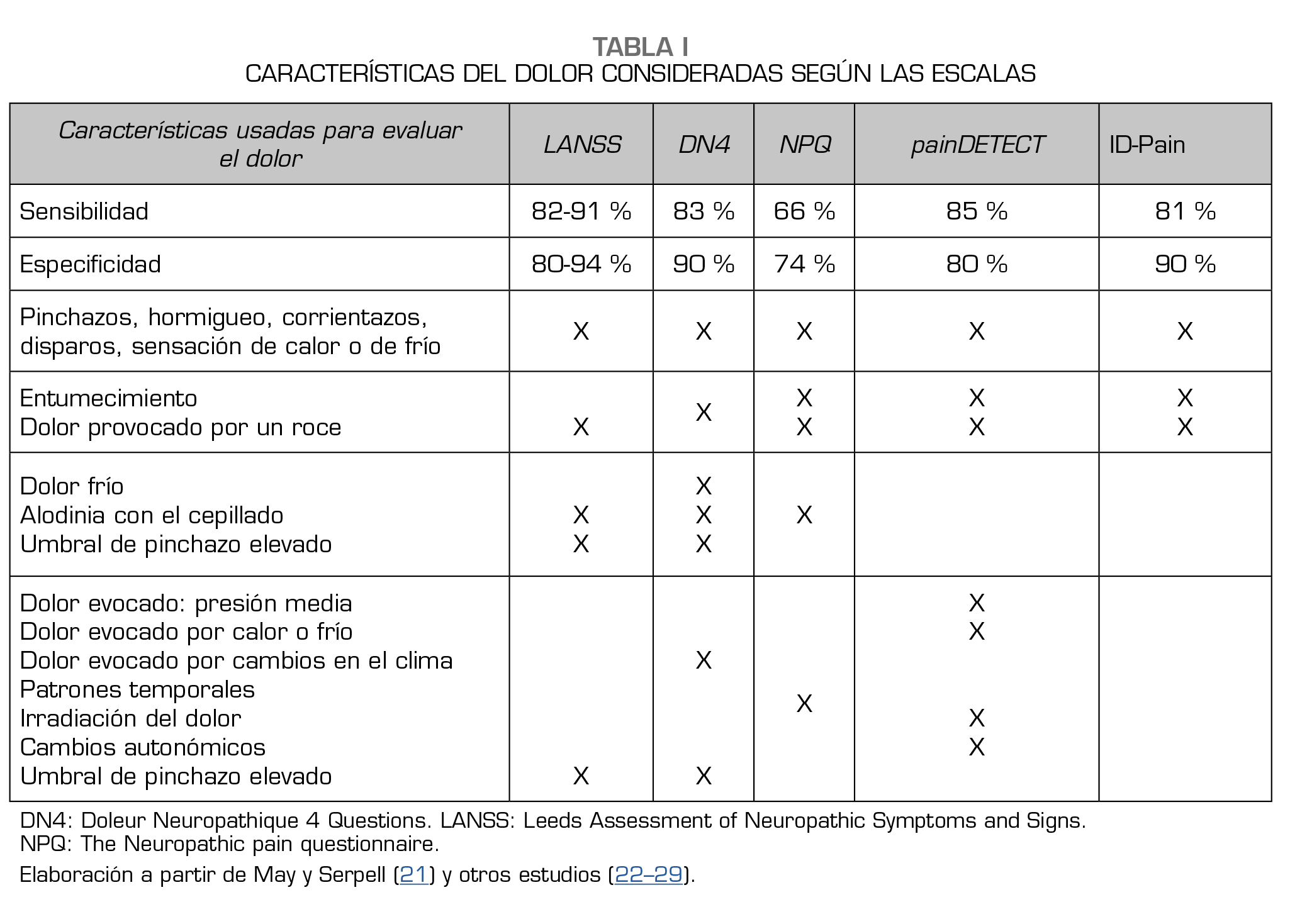
La guía de NEUPSIG para el diagnóstico del dolor neuropático sugiere algunas herramientas de evaluación como el The Leeds Assessment of Neuropathic Symptoms and Signs (LANSS) que consta de 5 ítems de síntomas y 2 de examen físico, y de una escala de LANSS autorreportada, con una sensibilidad del 82-91 % y una especificidad del 80-94 % (22,23,24). La escala The Neuropathic pain questionnaire (NPQ) es una escala de 12 ítems, 10 de ellos describen síntomas y 2 están relacionados con el afecto: esta es útil al ayudarnos a diferenciar un dolor neuropático de uno que no lo es, cuenta con una sensibilidad del 66 % y una especificidad del 74 % (25). Otra escala es Doleur Neuropathique 4 Questions (DN4), consta de 10 ítems, 7 sobre síntomas y 3 con base en el examen físico, un puntaje de 4 a 10 indica dolor neuropático, cuenta con una sensibilidad del 83 % y una especificidad del 90 % (26). La escala painDETECT fue desarrollada en Alemania, consta de 9 ítems y no requiere de examen físico, cuenta con una sensibilidad del 85 % y una especificidad del 80 % (27). Y el ID-Pain es una escala con 5 descriptores sensoriales del dolor y un ítem relacionado con si el dolor se ubica en las articulaciones, no requiere examen físico y su propósito es identificar si el dolor tiene un componente neuropático, siendo su punto de corte ≥ 3 (28,29).
El cuestionado ID-Pain se desarrolló en el año 2006 por medio de un comité en Nueva York donde participaron especialistas como neurólogos, anestesiólogos y reumatólogos, además médicos de atención primaria, con el objetivo de desarrollar una herramienta que pudiera diferenciar el dolor neuropático del nociceptivo. Para esto se realizó un estudio multicéntrico que incluyó 308 pacientes (105 pacientes con dolor neuropático, 99 con dolor nociceptivo y 104 pacientes con dolor tanto neuropático como nociceptivo), para así validar el instrumento. El coeficiente intelectual de la escala fue de 0,72, siendo su intervalo de confianza al 95 % entre 0,667 y 0,795), lo que significa que tiene un buen rendimiento en la identificación del dolor neuropático, siendo el ítem con mejor desempeño la sensación de adormecimiento (28). Esta escala cuenta con validación al castellano, y se caracteriza por ser un cuestionario breve, autoadministrado, que puede detectar de forma rápida un dolor neuropático. Aunque ninguna de estas escalas aborda directamente el DMF, las características enunciadas pudieran ser de utilidad en la clínica, contando con una sensibilidad de 81 % y una especificidad del 90 %, además de un área bajo la curva de eficacia diagnóstica del 90 % (28).
La Tabla 1 resume las características del dolor consideradas según las escalas, siendo los síntomas más comunes evaluados en estas los de pinchazo, hormigueo, corrientazo, disparos y sensación de calor o de frío (21).
TRATAMIENTO
Tratamiento farmacológico
El consenso de expertos de Delphi concluyó que los tratamientos farmacológicos con mayor evidencia y apoyados por los especialistas encuestados fueron la amitriptilina, pregabalina, gabapentina, morfina, ketamina, infusión intraforaminal de lidocaína, y antinflamatorios no esteroideos, siendo tan solo la amitriptilina la que se recomienda con un nivel de consenso moderado (17). El objetivo del tratamiento farmacológico es el control sintomático, principalmente el dolor. Entre los analgésicos, aunque con pobre evidencia, los antinflamatorios no esteroideos pueden ser usados en ciclos cortos para disminuir los efectos adversos renales, cardiovasculares y gastrointestinales (30).
Los opioides fuertes y débiles se han usado en dolor neuropático, tienen una efectividad demostrada de un 0,27 con un intervalo de confianza entre 0,16-0,38, sin embargo, hay que usarlos con precaución en dolor crónico por el riesgo de dependencia, como lo demostró el metanálisis de Cochrane (31). Algunos estudios han investigado el uso de tapentadol (32), y otros de metadona, en conjunto de fármacos neuromoduladores (1,3). Otros estudios han mostrado la efectividad de morfina en el DMF. Uno de ellos usó morfina por vía oral en un rango de 70-300 mg/día, demostrando una disminución del dolor de hasta el 42 % y un 8 % de respuesta parcial; y en estudios de resonancia magnética funcional sugería reducción en la reorganización cortical (33,34). Otro de ellos mostró la efectividad de la morfina oral (15 mg iniciales de morfina de liberación sostenida), que fue titulada en el manejo del DMF con número necesario a tratar para disminución del 50 % de 5,6 y del 33 % del dolor del 4,5, comparado con mexiletina y placebo (35,36). Los efectos adversosmás frecuentes fueron cansancio, mareos, sudoración, estreñimiento, retención urinaria, náuseas, vértigo, prurito, entre otros (31,37).
Con respecto a los gabapentinoides, se identificaron dos ensayos clínicos aleatorizados (ECA). El estudio de Bone y cols. correspondió a un ensayo doble ciego, cruzado, que comparó gabapentina (hasta 2400 mg) frente a placebo, observándose una disminución del dolor en ambos grupos; aunque la reducción fue mayor con gabapentina (3,2 vs. 1,6), la diferencia no alcanzó significación estadística (38). Por su parte, Smith y cols. incluyeron 24 pacientes con dolor de miembro fantasma y dolor residual del muñón, administrando gabapentina hasta una dosis máxima de 3600 mg, y encontraron una reducción del dolor del DMF frente a placebo, sin diferencias estadísticamente significativas (39). No obstante, la revisión Cochrane que combinó los resultados de ambos estudios evidenció una mejoría estadísticamente significativa en las puntuaciones de dolor (37).
Con respecto a los antidepresivos, la evidencia es inconsistente, y los estudios cuentan con poco número de pacientes. Los antidepresivos tricíclicos, pese a que son ampliamente usados en dolor neuropático, no han demostrado efectividad en DMF (40); un ECA comparó amitriptilina con placebo por 6 semanas en 39 pacientes, sin obtener resultados estadísticamente significativos, siendo los efectos adversos mayores en el grupo de intervención como xerostomía, visión borrosa, somnolencia, estreñimiento, náuseas, vómito y retención urinaria (41). La mirtazapina, un antagonista alfa 2 que mejora la transmisión noradrenérgica al bloquear la inhibición de la liberación presináptica de norepinefrina, y una mayor especificidad por la modulación de los 5TH 1 (agonismo), 5TH2 y 3 (antagonismo) en una serie de casos demostró una eficacia en la reducción del dolor superior al 50 % y con menos efectos secundarios que los antidepresivos tricíclicos (42).
Adicionalmente los antidepresivos duales han mostrado eficacia en manejo de dolor neuropático, pero existe una escasa evidencia en el escenario específico de DMF (20,40). Para duloxetina solo se cuenta con un reporte de caso (43) que demuestra efectividad junto con pregabalina. Con venlafaxina no encontramos estudios, y se cuenta con 2 reportes de caso de milnacripran (44,45).
Entre los antagonistas del receptor NMDA estudiados para DMF están la ketamina, la memantina y el dextrometorfano (40). La memantina cuenta con 3 ECA incluidos en la revisión de Cochrane, en los que no se pudo comprobar su efectividad y con algunas limitaciones en el análisis estadístico (40,46,47,48), encontrándose un ECA para manejo de DMF agudo en que sí fue efectivo en conjunto con bloqueo del plexo braquial (49,50). El dextrometorfano contó con un estudio de 10 pacientes con amputaciones secundarias a patologías oncológicas, en los que se suministraron 60 mg/ 2 veces al día (un participante tuvo 90 mg/2 veces por día) demostrando un alivio del dolor del 50 % (51).
La ketamina ha mostrado efectividad en la reducción del dolor neuropático reduciendo el proceso de sensibilización central, y en consecuencia la hiperalgesia y alodinia. Se cuenta con dos ECA, el primero se hizo comparando ketamina en infusión (0,5 mg/kg) con placebo, demostrando efectividad en reducción del dolor del muñón y de miembro fantasma con ketamina por encima de placebo (52). El segundo ECA suministró a pacientes con DMF una infusión de ketamina de 0,4 mg/kg, a otros una infusión de calcitonina 200 IE y un tercer brazo dio las dos infusiones al mismo tiempo, encontrándose efectividad en la ketamina en la reducción del DMF en monoterapia, ya que se comprobó que la terapia combinada no ofrecía beneficio, siendo la acción sobre la sensibilización central la clave de la efectividad de la ketamina (53). Como efectos adversos se encontró pérdida de la conciencia, sedación, alucinaciones visuales y elevación del ánimo (37).
Tratamientos no farmacológicos
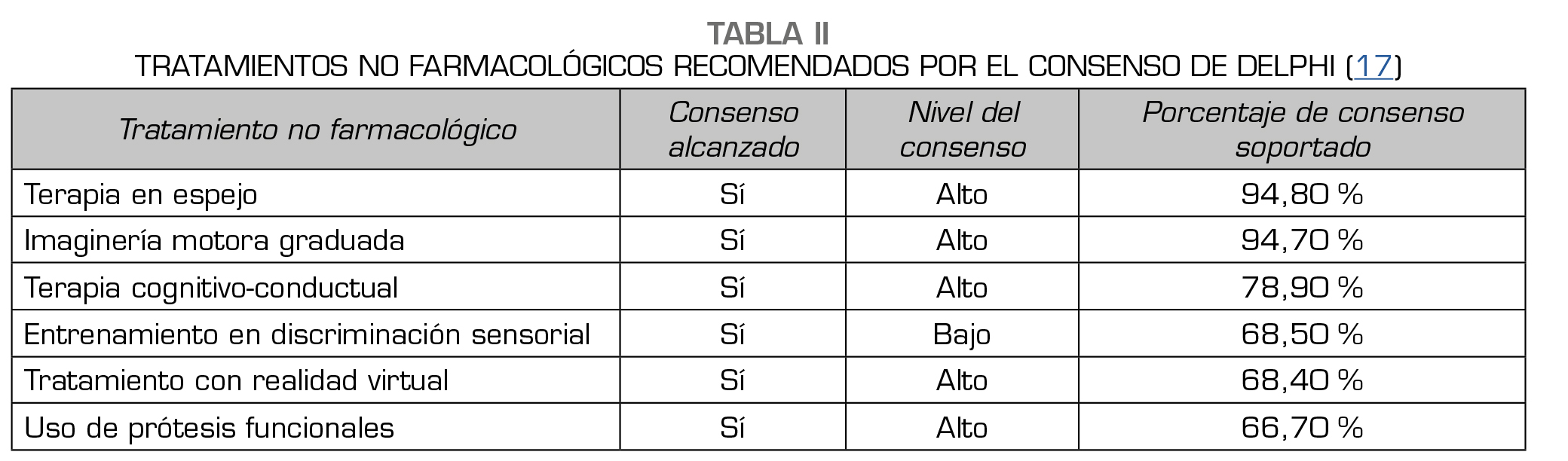
El consenso de Delphi concluyó entre los tratamientos no farmacológicos seis estrategias con evidencia científica y eficaces en la práctica clínica. Entre estas, la TE fue la de mayor evidencia, seguido por imágenes motoras graduadas, terapia cognitivo-conductual, uso de prótesis funcional, entrenamiento de discriminación sensorial y entrenamiento en realidad virtual (17) (Tabla 2).
Terapia en espejo
Esta técnica fue implementada por primera vez hacia el año 1996 con los trabajos de Ramachandran, quien hizo el primer ensayo clínico, obteniendo resultados satisfactorios en disminución de dolor, mejoría en posición de congelamiento y en sensación de miembro fantasma, incluso con el fenómeno de telescoping (19). El desarrollo de la idea partió de una comprensión de que se debía trabajar sobre los mecanismos centrales, con una representación visual de la extremidad, pensando la caja del espejo como una “caja de realidad virtual” (19,54). La TE consiste en poner la extremidad intacta en un espejo mientras el muñón se coloca detrás del espejo. Así se crea la ilusión de tener ambas extremidades, y se realizan ejercicios (17).
Se destaca por ser una terapia fácil de llevar a cabo, económica y segura. Sin embargo, se reportan algunos efectos adversos, que puede ir desde mareo en un 58 %, irritación en un 18 %, e inquietud hasta en un 12 % (55). Se considera que la efectividad de esta técnica radica en la reintegración de los sistemas sensorial y motor, la modulación del miedo al movimiento y la restauración del esquema corporal, actuando sobre los procesos de reorganización cortical desadaptativa. Asimismo, la observación del movimiento favorece la activación del sistema de neuronas espejo, lo que genera una percepción del movimiento, mejora la propiocepción y proporciona retroalimentación visual, incrementando la excitabilidad motora y cortical y contribuyendo, en última instancia, a la reducción del dolor (56).
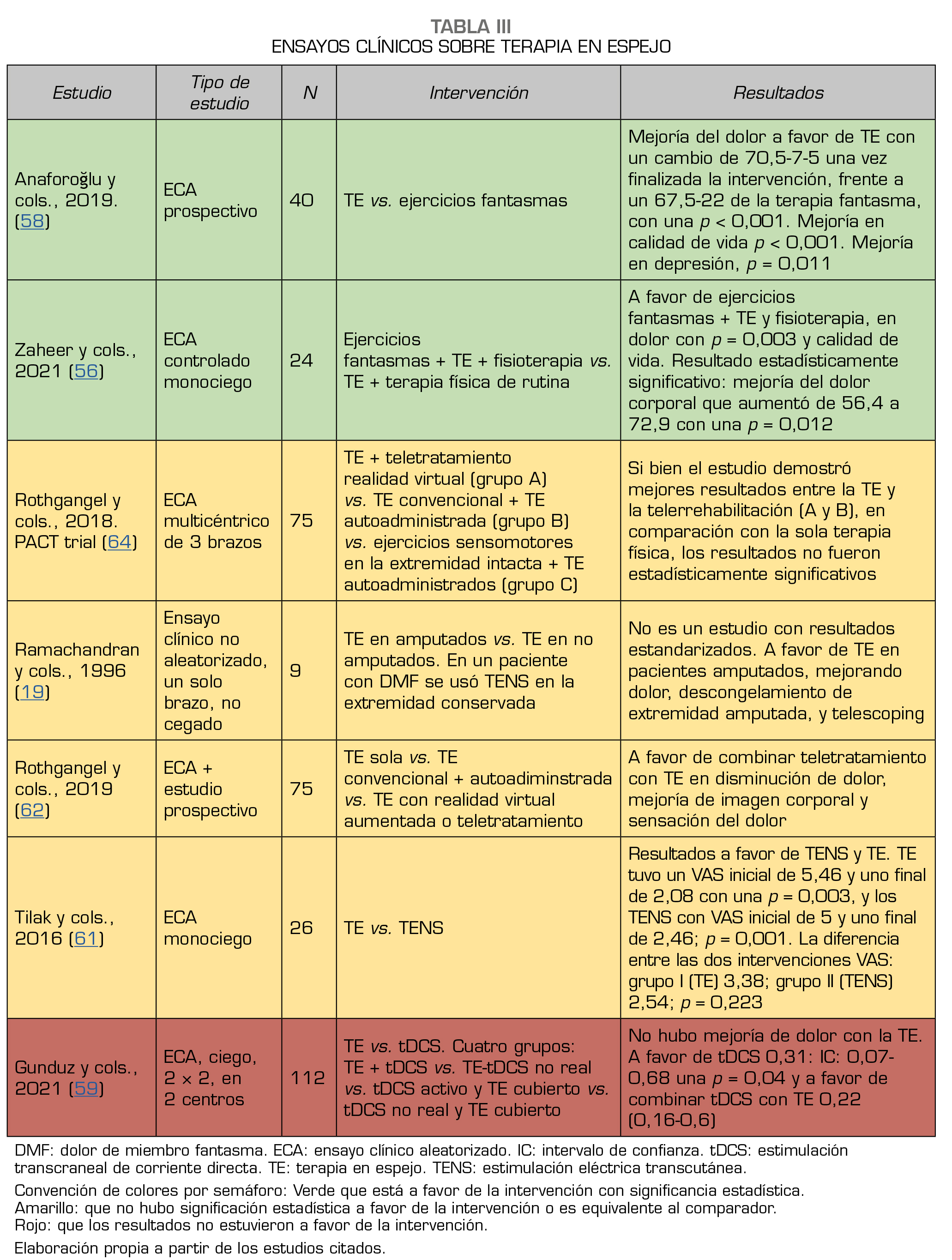
Xie y cols. realizaron un metanálisis de 10 ECA, en los que se logró demostrar que la mejoría del dolor usando esta técnica se daba a un mes, y con una terapia mayor a un año, con una medida de asociación de −0,46 intervalo de confianza de –0,85--0,07 y una p de 0,02, sin embargo, no hubo una mejoría significativa en los ECA que arrojaron resultados a los 3, 6 meses y menos de un año (57). En los estudios revisados, encontramos que la TE es superior cuando se compara con los ejercicios fantasma (58), pero es inferior cuando se compara con técnicas como la estimulación transcraneal por corriente directa (59), sin embargo, cuando se integra la TE a los ejercicios fantasma, es superior a la terapia física convencional (56).
Otra revisión sistemática de la literatura de Campo-Prieto y cols. concluye que, aunque se ha demostrado que la TE ha facilitado la reducción del DMF, en algunos casos esta mejora no se puede atribuir solo a la TE. El tiempo en el que se administra esta terapia es de suma importancia, puesto que se ven mejores resultados cuando se administra a largo plazo, y combinando esta terapia con otras técnicas. Nuevamente se pone en cuestión la necesidad de acompañar este tipo de terapia con otras o con tratamiento farmacológico (60).
Por ejemplo, unos de los estudios combinaron estimulación eléctrica transcutánea (TENS) con TE, lo cual demostró mayor efectividad en el alivio del dolor (61). Otros estudios apoyan la TE con telerrehabilitación, con el propósito de que se pueda garantizar estrategias que se sostengan en el tiempo y que se pueda realizar desde casa. Los ejercicios de teletratamiento incluyen monitorización del DMF, programas de ejercicios digitales utilizando la TE tradicional, uso de la realidad aumentada con la TE, entrenamiento de reconocimiento de lateralidad en extremidades (62,63). Se hizo un estudio de tres brazos, en el que pese a que se demostró mejoría del dolor con la TE y la TE más la telerrehabilitación, frente a la terapia física, los resultados no tuvieron significación estadística (64) (Tabla 3).
Ejercicios fantasmas
La ejecución motora fantasma, o ejercicios fantasmas, consiste en el movimiento imaginario de un miembro fantasma en el cerebro, junto con la realización de ciertos movimientos físicos reales de la extremidad intacta, el movimiento de ambas extremidades en dirección opuesta, el reposicionamento y los movimientos articulares, que ayudan a aliviar el DMF de forma segura. Fue presentada por primera vez por el profesor turco Ülger y su equipo en el año 2009, profesor en Turquía, por medio de un estudio piloto en el que comparaba los ejercicios fantasmas y de prótesis con ejercicios convencionales más de prótesis, encontrando una mejoría significativa de DMF con una p < 0,05 vs. ejercicios convencionales (65).
Como evidenciábamos previamente, cuando se integran los ejercicios fantasmas a la TE es superior a la sola terapia física convencional. Sin embargo, se requiere al menos un tiempo de cuatro semanas para obtener resultados, ya que en las dos primeras semanas algunos pacientes experimentaron el fenómeno de fantasma paralizado, consiguiendo con el tiempo el entrenamiento y la movilización del miembro fantasma. Esto a su vez impacta en la reorganización cortical, en que por medio de los ejercicios imaginarios se engaña al cerebro, haciendo ver que se puede mover el miembro fantasma y que este es indoloro, reduciendo en consecuencia el dolor como demostró el estudio de Zaheer y cols. (56).
Imaginería motora graduada
La imaginería motora graduada se basa en las alteraciones en la representación de la corteza sensorial, premotora y motora de la extremidad amputada, proporcionando un programa de tres pasos que aborda dichos cambios desadaptativos, mediante restauración de la lateralidad, movimientos imaginados y TE. La primera estrategia implica que cuando se debe distinguir una parte del cuerpo que pertenece a un lado, por ejemplo, el izquierdo, se activa la corteza somatosensorial, premotora y motora, y también la de la extremidad contralateral como áreas suplementarias contralaterales. Los movimientos imaginados implican imaginar mover el miembro fantasma en varias posturas, y la TE se integra a esta terapia proporcionando la retroalimentación visual con la intención motora, resolviendo el desajuste vasomotor que puede contribuir al dolor (66).
Esta técnica busca activar las neuronas en espejo, y restablecer la organización cortical, actuando a nivel central accediendo al cerebro a través de su neuromatriz corporal (67). Sobre la efectividad de esta técnica, se cuenta solo con tres ECA. El más reciente es el de Limakatso y cols. (2020), en el que se tomó un grupo de 21 adultos con amputaciones y DMF, comparando un programa de imaginería motora graduada con fisioterapia de rutina durante seis semanas, evaluando los desenlaces de mejoría del dolor y calidad de vida en seis semanas, tres meses y seis meses, con medidas de asociación a favor de esta técnica, aunque con unos intervalos de confianza muy amplios, esto debido a lo pequeña que era la muestra (68) (Tabla 4).

Estimulación eléctrica transcutánea
La TENS ha demostrado efectividad a baja frecuencia y alta intensidad (3). Esta terapia responde a la compresión de los mecanismos periféricos del DMF; los estudios de Vaso y cols. explican cómo se da un fenómeno de la periferia hacia el sistema nervioso central (contrario a la mayoría de explicaciones de DMF que sustentan teorías del centro a la periferia) cuando se provoca la amputación, lo que lleva a una entrada exagerada de señales ectópicas al ganglio de la raíz dorsal, generando los cambios desadaptativos (69). Esto sustenta la importancia de intervenciones periféricas como son las TENS, en las que se ponen electrodos en la raíz nerviosa, o a lo largo del nervio que inerva el área dolorosa. El estudio de Mulvey y cols. se hizo con uso de TENS en muñón, encontrándose disminución del dolor del muñón tanto en reposo como en movimiento, aunque también se evidenció un aumento de la sensación de miembro fantasma (70).
Un estudio de caso de un hombre de 36 años, con dolor agudo de miembro fantasma, mostró alivio del dolor y una mayor conciencia del miembro fantasma gracias a una terapia con TENS en la que se administró una alta frecuencia (100 Hz) durante 15 min, seguidos de TENS de baja frecuencia (10 Hz) durante otros 15 min, una vez al día durante 3 días consecutivos. La alta frecuencia proporciona analgesia, hecho explicado por el mecanismo de teoría de la compuerta, al activar las fibras A-Beta de conducción rápida, mielinizadas, que compiten con la transmisión del estímulo nociceptivo de las fibras C de conducción lenta amielínicas. A su vez la baja frecuencia proporciona analgesia al activar los receptores opioides en la periferia y el asta dorsal de la médula espinal. Se ha demostrado que este tipo de intervención es económica y con pocos efectos adversos, recomendada principalmente en DMF agudo (71).
Realidad virtual
Partiendo de la importancia de los mecanismos centrales, y de la “plasticidad desadaptativa”, la reorganización cortical en la corteza sensorial y motora posterior a la amputación sustenta el DMF y la importancia de los mecanismos de representación sensorial de la extremidad faltante, como es el uso de realidad virtual (72). El área cortical de la extremidad faltante comienza a responder a zonas contiguas que invaden dicha corteza. Como se ha demostrado en los estudios de resonancia magnética funcional, la zona contigua a la mano corresponde al labio, por lo que la gravedad del DMF se corresponde a la invasión del área cortical por el área contigua (73). El estudio de Ichinose y cols. precisamente demuestra cómo a través de la realidad virtual en pacientes con amputación de miembro superior, pero incluyendo estímulos táctiles puede generarse mejoría del DMF, cuando el estímulo se provoca en la mejilla, más que en la extremidad contralateral, acompañado de realidad virtual que representa la extremidad faltante (74).
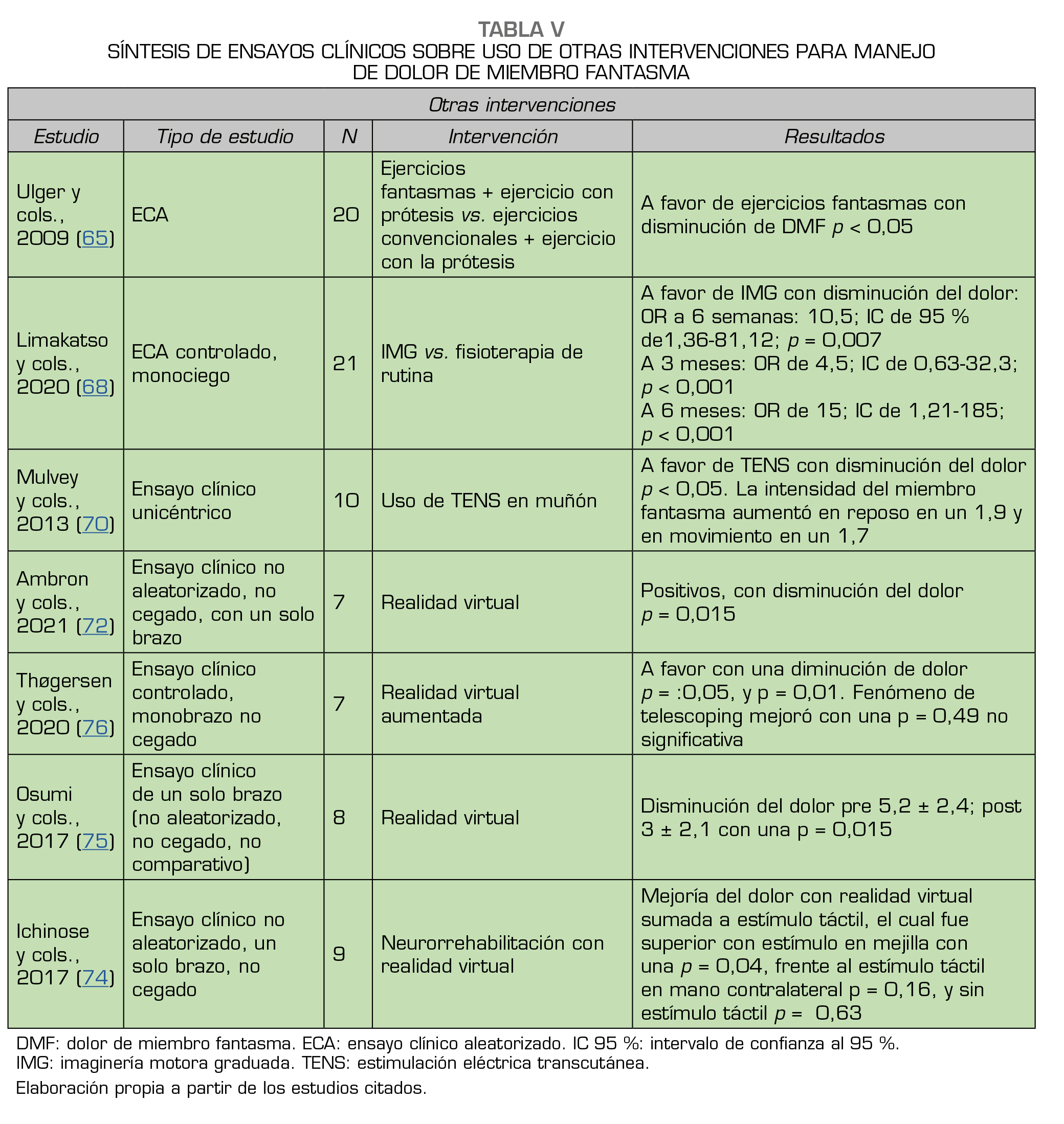
Los ensayos clínicos con realidad virtual han tenido buenos resultados, encontrando mejoría del dolor (72,74,75,76). Estos han incluido, además de las imágenes por realidad virtual, otro tipo de estímulos sensoriales, como el táctil (72,74), encontrándose una mejoría del dolor cuando se incluye el estímulo táctil vs. cuando no se incluye (72), y cuando este se provoca en el rostro, cuando la amputación es de miembro superior (74) (Tabla 5).
Terapia psicológica
El estrés psicológico es un desencadenante del DMF y exacerba los episodios de dolor, además se considera el DMF como un proceso de aprendizaje y de memoria desadaptativos del cerebro (1,5). Sin embargo, no se considera que sea un fenómeno eminentemente psicológico, o que incluso corresponda a trastornos mentales o de personalidad, como en algún momento se afirmó hacia la década de 1970 (1,5). La amputación como fenómeno per se es un evento de gran magnitud para la salud mental del sujeto, por lo que hasta un 20-60 % de los pacientes amputados pueden ser diagnosticados con síntomas depresivos. Adicionalmente, algunos factores cognitivos desempeñan un papel en la modulación del DMF. Así, si una persona tiene pocas estrategias de afrontamiento, es negativa y catastrofista puede desarrollar más DMF y tiene una menor respuesta a los tratamientos (13). Por esto se habla de la importancia de la preparación en la educación al paciente y el manejo del estrés antes de la amputación. Una vez se establece el DMF se han descrito la hipnoterapia y la terapia cognitivo-conductual. Los factores psicosociales pueden aumentar el dolor e inducir cambios desadaptativos cerebrales, por tanto, la terapia psicológica debe ir enfocada a ellos (15).
No existe una alta evidencia de la terapia cognitivo-conductual en el manejo específico del DMF. Sin embargo, el consenso de Delphi la avala como una de las estrategias útiles en el manejo, por su alta evidencia en el manejo de dolor crónico y la efectividad en la práctica clínica. Parece que el principio central de la terapia cognitivo-conductual actual sobre la teoría del dolor por la neuromatriz, que enfatizan en el papel de las influencias cognitivas, afectivas y conductuales en el desarrollo y mantenimiento del dolor crónico (17). La terapia cognitivo conductual tiene como objetivo reducir la expresión del dolor y permitir que el paciente pueda hacer movimientos y posturas normales; busca, entonces, cuestionar la espiral negativa de la conducta dolorosa y reforzar las conductas saludables. Esta terapia también orienta a usar medicación y terapias por horario, y no cuando se presente el dolor, para disminuir la relación entre procesos negativos, dolor y estrategias analgésicas y de terapia. Propende el cambiar pensamientos y actitudes que aumentan el dolor, practicar estrategias de manejo de dolor como redirección de la atención, resolución de problemas, y entrenamiento en exposición al miedo al dolor. En algunos casos se sirve de las técnicas de biorretroalimentación, en que se miden las variables fisiológicas como temperatura, tensión muscular, frecuencia cardiaca, enseñando al paciente a regularlas (15).
Uso de prótesis funcionales
El uso de prótesis, más aún mioeléctricas, disminuye la reorganización cortical y mejora el DMF, ya que sugieren una retroalimentación visual y sensorial (15). El consenso de Delphi apoya el uso de prótesis funcional pese a la falta de evidencia científica (17). La prótesis proporciona una retroalimentación propioceptiva, visual y funcional al muñón durante las actividades funcionales como, por ejemplo, caminar o coger un objeto. La literatura ha demostrado la superioridad de una prótesis funcional frente a una prótesis cosmética en la mejoría del dolor y de función. De hecho, puede incidir en mejorar la reorganización cortical, al proporcionar una retroalimentación somatosensorial (77).
Otras técnicas
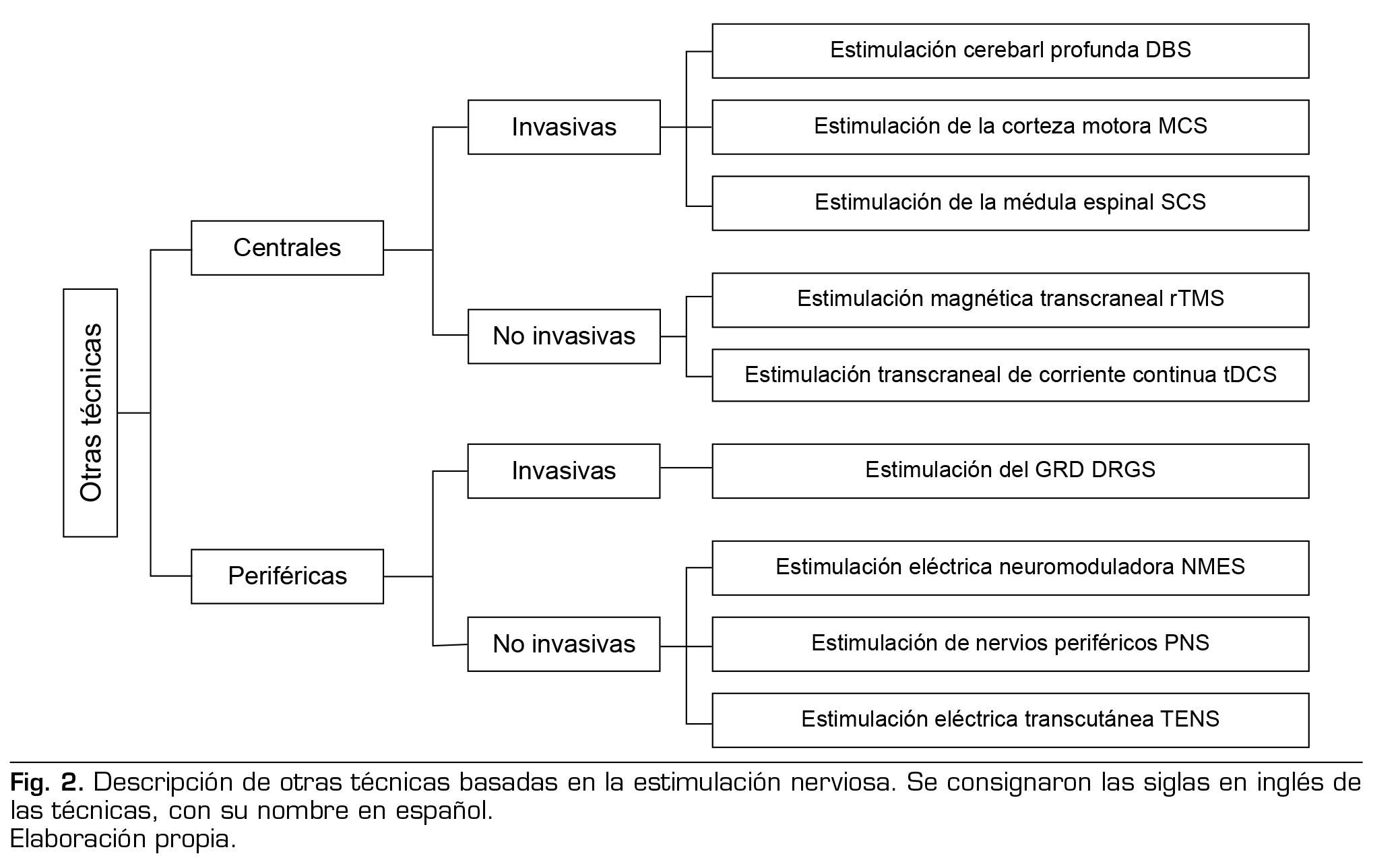
Se han descrito intervenciones invasivas centrales como la estimulación cerebral profunda, la estimulación de la corteza motora) y la estimulación de la médula espinal; y periféricas, como la estimulación del ganglio de la raíz dorsal. Asimismo, estimulaciones centrales no invasivas como la estimulación magnética transcraneal, la estimulación transcraneal de corriente directa, incidiendo en la reorganización cortical maladaptativa anteriormente descrita (9,78). Además, técnicas periféricas como TENS, estimulación eléctrica neuromoduladora y estimulación de nervios periféricos. Esta estimulación periférica activa las fibras A-Beta lo cual mitiga la actividad nociceptiva de las fibras A-Delta y de las fibras C, inhibiendo las vías del dolor por la médula espinal, generando su efecto analgésico (78). En una revisión sistemática con un total de 123 pacientes, encontraron que las técnicas de estimulación central no invasivas tenían una buena evidencia en cuanto a disminución del dolor, siendo la estimulación transcraneal de corriente directa la de mejor rendimiento estadístico tanto a corto como a largo plazo frente la estimulación magnética transcraneal, con una frecuencia de 10 Hz (79) (Figura 2).
CONCLUSIONES
El dolor de miembro fantasma (DMF) es un fenómeno descrito desde el Renacimiento; sin embargo, pese al paso de los siglos, sus mecanismos fisiopatológicos aún no se comprenden completamente. Tradicionalmente se ha clasificado como un tipo de dolor neuropático debido al daño nervioso y a las sensaciones dolorosas referidas por los pacientes; no obstante, puede considerarse una entidad clínica particular, con características propias y procesos fisiopatológicos que trascienden los del dolor neuropático clásico, como la reorganización cortical y la participación de la neuromatriz del dolor. Los mecanismos fisiopatológicos se dividen en periféricos y centrales. Los periféricos son los relativos al daño de nervio o segunda neurona, y los centrales a las transformaciones cerebrales que ocurren posterior a la amputación. Son los mecanismos centrales los que hasta el momento han explicado mejor el DMF y los que justifican la mayoría de los tratamientos tanto farmacológicos como no farmacológicos.
Los factores de riesgo asociados al desarrollo de DMF incluyen un inadecuado control del dolor preoperatorio y perioperatorio, la presencia de dolor residual del muñón, la formación de neuromas y determinadas actitudes frente al dolor. La identificación del DMF requiere una adecuada valoración clínica, sin embargo, no contamos con escalas específicas para esta entidad, por lo que se usan escalas para dolor neuropático en general, como LANSS, DN4, NPQ, painDETECT, e ID-Pain. De estas; una de las más estudiadas y validadas al español es la de LANSS, sin embargo, resaltamos la de ID-Pain porque se encuentra validada en nuestro idioma, cuenta con una buena sensibilidad y especificidad, y es fácil y sencilla de usar.
A nivel de tratamiento del DMF encontramos estrategias farmacológicas y no farmacológicas, siendo estas últimas las que mejores resultados a largo plazo ofrecen. Entre las estrategias farmacológicas las que mayor evidencia tienen son el uso de opioides principalmente aquellos con efecto dual (noradrenérgico y serotoninérgico); los gabapentinoides y los antagonistas de los receptores NMDA. Aunque los antidepresivos son de amplio uso en el dolor neuropático, hacen falta más estudios específicos con DMF, ya que en algunos casos se limitan a estudios de caso. Pese a que el consenso de Delphi sugiere los antidepresivos tricíclicos, un metanálisis de Cochrane no demostró un beneficio estadísticamente significativo con amitriptilina, mientras que sí evidenció mejoría en el control del dolor con gabapentinoides. A su vez los antagonistas de NMDA, específicamente la ketamina, han demostrado resultados prometedores, pero aún se requieren más estudios.
Entre las estrategias no farmacológicas resaltamos la TE como una de las técnicas más antiguas, estudiadas, costo-efectivas y sencillas de realizar que han demostrado mejoría en DMF. Su efectividad aumenta cuando se combina con otras intervenciones, tanto farmacológicas como no farmacológicas, como los ejercicios fantasmas, la realidad virtual y las técnicas de neuroestimulación. La imaginería motora graduada ha demostrado muy buenos resultados, y es una terapia que combina la TE con otras técnicas que promueven el ordenamiento cortical; asimismo la realidad virtual asociada a estimulación táctil ha demostrado buenos resultados. Adicionalmente, las prótesis mioeléctricas tienen un impacto positivo más que las cosméticas en prevenir y en tratar el DMF.
Las intervenciones psicológicas son fundamentales, ya que están implicadas en los factores predisponentes y desencadenantes del DMF. Al respecto, la más usada es la terapia cognitivo-conductual, que tiene una alta evidencia en manejo de dolor crónico. Existen otras técnicas descritas que promueven la estimulación nerviosa tanto central como periférica, tanto invasivas como no invasivas, siendo estas últimas las que han demostrado mejores resultados. Finalmente, esta revisión pone de manifiesto la necesidad de continuar investigando el DMF con el fin de comprender mejor sus mecanismos fisiopatológicos y de desarrollar estudios con mayor calidad metodológica, que permitan fortalecer el sustento científico y orientar la toma de decisiones clínicas más allá de las recomendaciones basadas en consenso de expertos.
CONFLICTO DE INTERESES
Ninguno.
FINANCIACIÓN
Ninguna.
BIBLIOGRAFÍA