10.20986/resed.2026.4212/2025
ORIGINAL
Uso de parche de capsaicina 8 % en dolor neuropático crónico refractario: estudio de dos series de casos
Use of capsaicin 8 % patch in refractory chronic neuropathic pain: study of two cases series
Gerardo Correa-Illanes1,2
Gerardo Correa-Torres3
Ruperto Correa-Torres4
Ana María Torres-Ubiergo2
César Margarit-Ferri5
1Unidad de Dolor. Hospital Clínico Mutual de Seguridad. Santiago, Chile
2Unidad de Dolor. Clínica RedSalud Providencia. Santiago, Chile
3Medicina Física y Rehabilitación. Universidad Mayor. Teletón. Santiago, Chile
4Endodoncia. Universidad de Valparaíso, Chile
5Unidad de Dolor. Hospital Gral. Universitario Dr. Balmis. Alicante, España
RESUMEN
Introducción: A pesar de los múltiples tratamientos orales e intervencionistas disponibles, el dolor neuropático localizado sigue siendo infratratado y presenta tasas de respuesta reducidas. El tratamiento tópico se ha constituido como una alternativa para diversas poblaciones de pacientes con dolor neuropático localizado.
Objetivos: Evaluar los resultados del uso repetido del parche de capsaicina al 8 % (PC8) en dolor neuropático localizado en la práctica clínica diaria, valorando la respuesta mediante dolor espontáneo, alodinia mecánica y área dolorosa tratada. Diseño del Estudio: estudio observacional, retrospectivo, descriptivo de series de casos. Lugar: todos los pacientes fueron tratados con PC8 en Clínica RedSalud Providencia o en Hospital Clínico Mutual de Seguridad CChC, Santiago de Chile entre 2022 y 2024.
Métodos: Se seleccionaron los pacientes con dolor neuropático localizado probable o definitivo, perfil sensitivo de ‘nociceptor irrititable’ (alodinia mecánica), y Cuestionario DN4 ≥ 3/7. El resultado primario de la eficacia terapéutica fue la disminución de la intensidad del dolor espontáneo, alodinia mecánica y tamaño del área dolorosa entre el estado basal y el último tratamiento. Se evaluó, además, mejoría en la calidad de vida, reducción de consumo concomitante de analgésicos orales y tolerabilidad del fármaco. Se realizaron evaluaciones mensuales, con aplicaciones periódicas de PC8 siguiendo las normas europeas y según la ficha técnica. Se evaluó calidad de vida con escala EuroQoL-5D-3L.
Resultados: De 12 pacientes analizados, en dos series de seis cada una, la primera presentó cicatrices dolorosas postraumáticas/postquirúrgicas con componente neuropático (‘Cicatrices’), y la segunda, neuralgia postherpética (‘NPH’). Se realizaron 3 o 4 aplicaciones de PC8 cada 3 meses, con seguimiento promedio de 10 meses en cada serie. Toda la serie ‘Cicatrices’ tuvo una reducción ≥ 30 % intensidad del dolor espontáneo basal y la mitad presentó reducción ≥ 50 %. Además, respecto a la intensidad de alodinia mecánica, la mitad presentó disminución ≥ 30%, y un tercio de la muestra ≥ 50 %. Todos los pacientes presentaron reducción del área dolorosa ≥ 50 %. En la serie ‘NPH’, respecto a la intensidad del dolor espontáneo basal, dos tercios de los pacientes tuvieron una reducción ≥ 30 % y la mitad una reducción ≥ 50 %. Asimismo, en relación con la intensidad de alodinia mecánica, la mitad tuvo una reducción ≥ 30 % y 1 paciente (17 %) disminución ≥ 50 %. Todos los pacientes presentaron reducción del área dolorosa ≥ 50 %. El 80 % de los pacientes de serie ‘Cicatrices’ y el 40 % de serie ‘NPH’ redujeron el consumo opioide gracias a combinación del tratamiento oral con PC8. Todos los pacientes mejoraron su calidad de vida y 11/12 pacientes (83 %) se reinsertaron socio-laboralmente al final del tratamiento.
Discusión: Se sugiere que el parche de capsaicina 8 % es una opción valiosa para el tratamiento del dolor neuropático localizado, proveyendo una reducción significativa de la intensidad del dolor espontáneo, alodinia mecánica y área dolorosa. Además, reduce el consumo de fármacos orales, particularmente opioides, y mejora la calidad de vida, acompañándose de buena tolerabilidad. Esta investigación tiene limitaciones inherentes a un estudio retrospectivo e incluye un pequeño número de pacientes, por lo que sugerimos la realización de estudios prospectivos con similar metodología y población, pero con mayor tamaño muestral.
Palabras clave: Capsaicina, dolor neuropático localizado, dolor crónico postquirúrgico, cicatriz, neuralgia postherpética
ABSTRACT
Introduction: Despite the multiple oral and interventional treatments available, localized neuropathic pain remains undertreated and has low response rates. Topical treatment has emerged as an alternative for various patient populations with localized neuropathic pain.
Objectives: To evaluate the results of repeated use of capsaicin patch 8 % (PC8) in localized neuropathic pain in daily clinical practice, assessing the response through spontaneous pain, mechanical allodynia and treated painful area. Study design: observational, retrospective, descriptive case series study. Setting: all patients were treated with PC8 at Clínica RedSalud Providencia or Hospital Clínico Mutual de Seguridad CChC, Santiago de Chile between 2022 and 2024.
Methods: Patients with probable or definite localized neuropathic pain, ‘irritable nociceptor’ sensory profile (static or dynamic mechanical allodynia), and DN4 Questionnaire ≥ 3/7 were selected. The primary outcome of therapeutic efficacy was the decrease in spontaneous pain intensity, mechanical allodynia and size of the painful area between baseline and the last treatment. Improvement in quality of life, reduction of concomitant consumption of oral analgesics and tolerability of the drug were also evaluated. Monthly evaluations were performed, with periodic applications of PC8 following European standards and according to the technical file. Quality of life was evaluated with the EuroQoL-5D-3L scale.
Results: Of 12 patients analyzed, in two series of six each, the first presented post-traumatic/post-surgical painful scars with neuropathic component (‘Scars’), and the second, post-herpetic neuralgia (‘PHN’). Three or four applications of PC8 were performed every 3 months, with an average follow-up of 10 months in each series. The entire ‘Scars’ series had a ≥ 30 % reduction in baseline spontaneous pain intensity and half had ≥ 50 % reduction. In addition, with respect to mechanical allodynia intensity, half presented ≥ 30 % decrease, and ? of the sample ≥ 50 %. All patients presented painful area contraction ≥ 50 %. In the ‘PHN’ series, with respect to baseline spontaneous pain intensity, ? of patients had a reduction ≥ 30 % and half had a reduction ≥ 50 %. Likewise, regarding mechanical allodynia intensity, half had a reduction ≥ 30 % and 1 patient (17 %) decrease ≥ 50 %. All patients presented painful area contraction ≥ 50 %. 80 % of patients in the ‘Scars’ series and 40 % in the ‘PHN’ series reduced opioid consumption due to combination of oral treatment with PC8. All patients improved their quality of life and 11/12 patients (83 %) were reintegrated socially and occupationally at the end of treatment.
Discussion: It is suggested that the capsaicin 8 % patch is a valuable option for the treatment of localized neuropathic pain, providing a significant reduction in spontaneous pain intensity, mechanical allodynia and painful area. In addition, it reduces the consumption of oral drugs, particularly opioids, and improves quality of life, accompanied by good tolerability. This research has limitations inherent to a retrospective study and includes a small number of patients, so prospective studies with similar methodology and population, but with a larger sample size, are suggested.
Key words: Capsaicin, localized neuropathic pain, chronic post-surgical pain, scar, postherpetic neuralgia
Correspondencia:
Gerardo Correa-Illanes
gerardo.correa01@gmail.com
Recibido: 13-05-2025
Aceptado: 04-01-2026
INTRODUCCIÓN
El dolor neuropático (DN) se origina como consecuencia directa de una lesión o enfermedad que afecta el sistema somatosensorial (1). Afecta a entre el 6,9 y el 8,2 % de la población de Europa (2,3) y al 10,1 % de los habitantes de Chile (4).
El DN se acompaña de deterioro significativo de la calidad de vida, afectando a la capacidad física, emocional, social y a la calidad del sueño (2,3). El DN crónico es una entidad de difícil tratamiento, siendo una importante proporción de pacientes refractarios a todas las terapias, manteniendo una respuesta parcial a pesar del uso de altas dosis de fármacos que actúan en el sistema nervioso central (SNC) y se asocian a una serie de eventos adversos (5).
El dolor en las cicatrices patológicas se observa en el 30-68 % de los casos; tiene generalmente características neuropáticas debido a la exposición prolongada y mayores niveles de factor de crecimiento neuronal (NGF) con crecimiento axonal directo, hiperinervación persistente e hiperexcitabilidad de fibras C peptidérgicas dentro de la cicatriz, asociado a presión física del colágeno sobre las fibras nerviosas, lo que causa neuropatía por atrapamiento intra-cicatrizal. Cirugías con alto riesgo de daño nervioso como las amputaciones y toracotomía a menudo cursan con más frecuencia con cicatrices dolorosas (6,7).
La neuralgia postherpética (NPH) corresponde al dolor persistente de más de tres meses de evolución desde la aparición de costras en las vesículas del herpes zóster (HZ). El daño inflamatorio de las neuronas aferentes primarias causa descarga espontánea, menor umbral de activación y respuestas exageradas a estímulos, con hiperexcitabilidad de las neuronas del asta dorsal, que sensibilizan al SNC. El 75 % de los pacientes con HZ sobre los 70 años desarrolla NPH. Además, la NPH tiene síntomas positivos que incluyen alodinia mecánica, disestesia e hiperalgesia. La sintomatología de la NPH es muy estresante y puede causar insomnio, depresión, bajada de peso y ansiedad (8).
La capsaicina es agonista selectivo del canal catiónico del Receptor de Potencial Transitorio Vaniloide 1 (TRPV1), aumentando la permeabilidad para el calcio. Este receptor polimodal se encuentra en las neuronas nociceptivas, especialmente fibras C amielínicas y débilmente en fibras A-Delta mielínicas. Inicialmente la capsaicina produce activación de los nociceptores cutáneos que expresan TRPV1, causando despolarización de las aferentes sensitivas, liberando neuropéptidos activos (especialmente sustancia P) e induciendo sensaciones de calor, quemazón, escozor y prurito de corta duración. La activación continua de los TRPV1 causa que los nociceptores hiperactivos de la piel pierdan parte de su sensibilidad a ciertos estímulos, prolongando su despolarización y provocando su desfuncionalización, asociándose a una reducción reversible de la densidad de fibras epidérmicas e inhibición del dolor. Este mecanismo se focaliza en los nociceptores que expresan TRPV1 sin afectar otras funciones sensitivas como la percepción del tacto o el frío (5,9,10). Los mecanismos subyacentes a la desfuncionalización inducida por capsaicina dependen de la concentración, donde dosis más altas pueden producir una desfuncionalización más rápida y prolongada de las fibras nociceptivas cutáneas, siendo este el fundamento detrás del uso del parche de capsaicina de alta concentración al 8 % (PC8), el cual al aplicarse durante una hora puede lograr hasta 3 meses de alivio del dolor. Se ha especulado que tratamientos repetidos con PC8 pueden aumentar las propiedades regenerativas del tejido nervioso, lo cual está por demostrarse. No se ha observado toxicidad acumulativa tras administraciones repetidas, siendo su absorción sistémica mínima, lo cual limita las potenciales interacciones medicamentosas o la necesidad de ajuste de dosis en pacientes ancianos o con insuficiencia hepática o renal (5,10,11).
Actualmente, en la Unión Europea el PC8 está aprobado para el tratamiento del DN periférico (DNP) en adultos, con cambio en la ficha técnica de 90 a 60 días, utilizándose solo o en combinación con otros medicamentos para el dolor (11).
En Chile el PC8 está aprobado para su uso clínico desde 2021. En 2022 se realizó una experiencia temprana en cinco centros de la ciudad de Santiago, apoyada por el laboratorio fabricante de PC8, siendo el primer país de Latinoamérica en iniciar su uso.
Para este estudio se optó por analizar dos series (NPH y cicatrices dolorosas) y describirlas por separado, debido a las diferencias existentes en aspectos biopsicosociales de los pacientes, tales como la edad, tiempo de evolución con dolor, fisiopatología, comorbilidades, fragilidad, contexto sociolaboral e indicaciones en ficha técnica, teniendo NPH abundante evidencia que avala su uso, en contraste con las cicatrices dolorosas, con escasa evidencia (12,13,14).
En la bibliografía revisada se puede evidenciar una deficiencia de información respecto a la reducción de la intensidad de la alodinia mecánica y del área dolorosa tras aplicaciones repetidas de PC8, lo cual apoyaría la realización de esta investigación.
El propósito del trabajo es describir la utilidad del parche de capsaicina al 8 % en el tratamiento tópico de pacientes portadores de cicatrices dolorosas de etiología postraumática/postquirúrgica con componente neuropático asociado y pacientes portadores de NPH, evaluando su efectividad, tolerabilidad y potencial reducción de consumo de fármacos analgésicos.
MATERIAL Y MÉTODOS
Diseño de investigación
Estudio observacional, descriptivo, retrospectivo de serie de casos, de corte transversal realizado en dos series de pacientes en centros de Santiago de Chile. La primera serie con cicatrices dolorosas postraumáticas/postquirúrgicas (Serie ‘Cicatrices’) atendidos en Unidad de dolor crónico del Instituto de Neurorehabilitación, Hospital Clínico Mutual de Seguridad CChC, y la otra serie de pacientes con neuralgia postherpética crónica (Serie ‘NPH’) atendidos en consulta ambulatoria de Clínica RedSalud Providencia.
Criterios de inclusión y exclusión
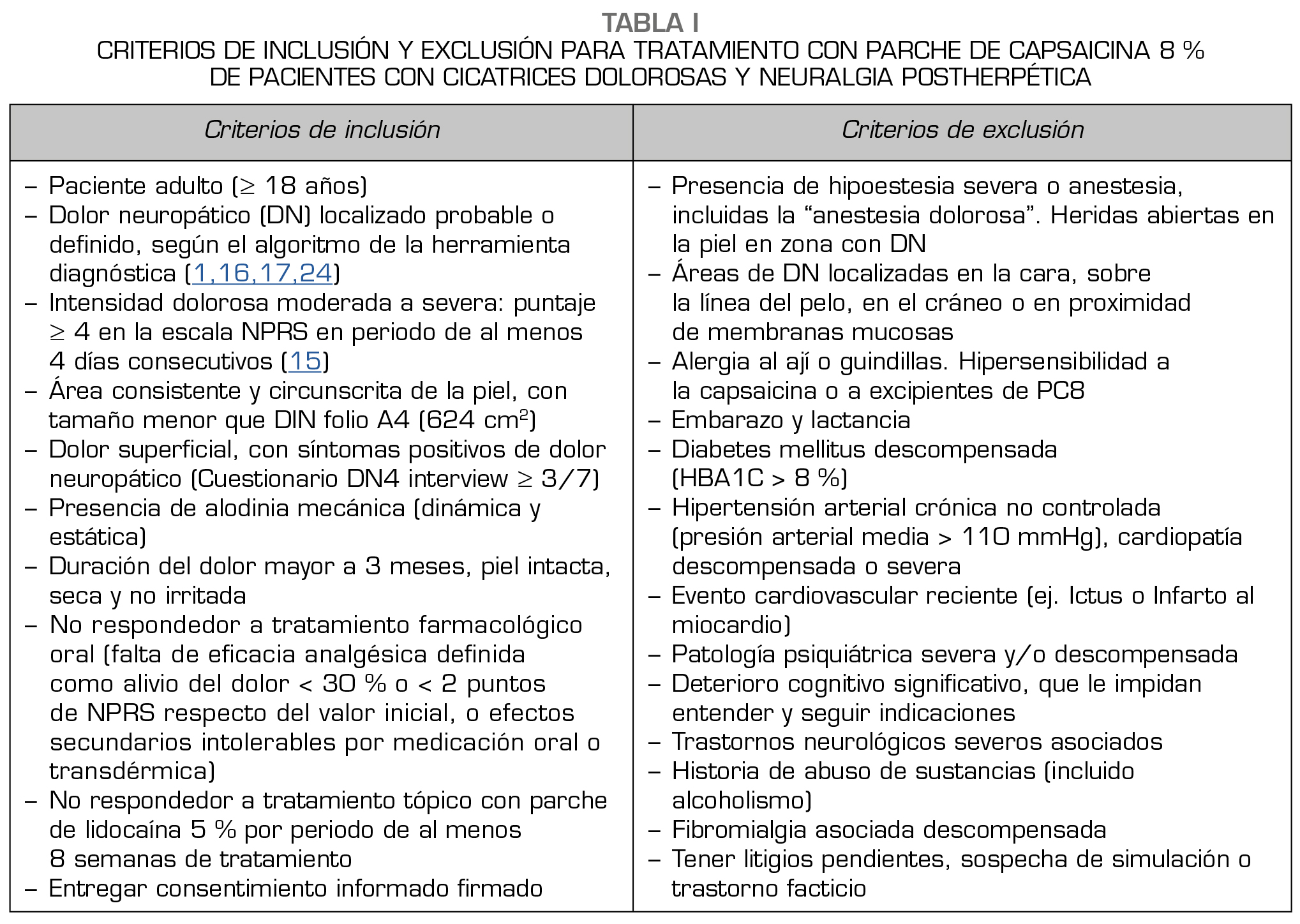
Los criterios de inclusión y exclusión se detallan en la Tabla 1.

Variables estudiadas
Intensidad de dolor espontáneo y evocado (alodinia mecánica): intensidad media de dolor, según la Escala de Valoración Numérica de Dolor medio (NPRS, mean Numerical Pain Rating Scale, en inglés).
Área dolorosa: evaluada por la presencia de alodinia mecánica estática (dolor evocado por presión ligera con el dedo índice) y/o alodinia mecánica dinámica (dolor provocado por roce suave con cepillo). La medición del área dolorosa se expresó en centímetros cuadrados (cm2).
En este estudio se utilizaron las siguientes herramientas clínicas:
Intervención
Se realizó evaluación de todos los pacientes por el mismo observador. Los resultados de la terapia fueron expresados como cambios absolutos o porcentuales en la escala de valoración numérica (NPRS), área de dolor, presencia e intensidad de alodinia mecánica, recuperación funcional, retorno sociolaboral, reducción del consumo de fármacos analgésicos, así como de efectos adversos secundarios a la medicación (22). Los pacientes fueron valorados mensualmente y el protocolo descrito fue aplicado en cada visita.
Se evaluó con la Escala EQ-5D-3L previo al inicio del tratamiento y al finalizar el estudio, determinando en cada caso los perfiles según su sistema descriptivo multidimensional.
Se realizó el mismo procedimiento de aplicación de PC8 a todos los pacientes de ambas series, el cual se describe en la Tabla 2.
Se realizaron 3 a 4 aplicaciones de PC8 en cada paciente, según la intensidad del dolor y respuesta al medicamento tópico. El tiempo de aplicación del PC8 fue de 60 minutos en todos los casos estudiados en ambas series de este estudio.
La terapia con PC8 fue definida como efectiva, considerando al paciente “Respondedor” a la terapia tópica si exhibía 1 o más de los siguientes resultados: disminución ≥ 30 % y/o disminución ≥ 2 puntos en escala NPRS desde el puntaje basal de dolor (8,10,22-24), y/o que presenta reducción ≥ 30 % en el área dolorosa inicial (25). Una mejoría en la funcionalidad fue considerada significativa si el paciente reportaba un aumento en su condición física que fuese social o laboralmente relevante (24).

Aspectos éticos
El estudio fue conducido de acuerdo con los principios de la Declaración de Helsinki y de Guías de Buenas Prácticas Clínicas. Se solicitó a todos los pacientes su consentimiento informado escrito para participar en esta investigación, en el cual se le entregó información detallada sobre el propósito del estudio, con explicación en lenguaje claro y sencillo, solicitando su autorización para acceder a su ficha clínica, recolectar la información de ella y para toma de fotografías de la zona de piel tratada, haciendo énfasis en el proceso de anonimización para asegurar la confidencialidad en el manejo de los datos y promoviendo una decisión independiente e informada del paciente, el cual tuvo la libertad de decidir aceptar o rechazar voluntariamente el uso de su información en cualquier momento del estudio.
El presente estudio tuvo la aprobación de los Comités de Ética Científica (CEC) de las instituciones de Santiago de Chile donde se realizó cada serie, CEC Mutual de Seguridad CChC resolución no. 389 y CEC RedSalud resolución no.P.1-2023.
Estudio estadístico
Para el análisis de variables cuantitativas, se utilizó media, desviación estándar, mediana y valores máximos y mínimos. Las variables cuantitativas se resumieron por medio de frecuencias absolutas y porcentajes relativos. Para comparar los valores medios en los mismos pacientes durante las dos fases de la investigación en cada serie se usaron test no paramétricos (test de Wilcoxon pareado). El coeficiente de correlación (r) fue usado para evaluar la correlación entre dos variables.
El análisis de los datos y elaboración de gráficos se realizó utilizando el programa StataCorp 2023 (Stata Statistical Software: Release 18. College Station, TX).
RESULTADOS
Entre junio de 2022 y mayo de 2024 se seleccionaron los pacientes de ambas series.
Serie ‘Cicatrices’
Datos demográficos
La población estudiada consistió en 5 hombres y una mujer, con edad promedio de 54,3 ± 6,3 (rango 48-64) años.
La causa subyacente fue cicatriz postquirúrgica en tres pacientes (toracotomía con reducción y osteosíntesis de fracturas costales; drenaje de hematoma glúteo y reducción y osteosíntesis de fractura de platillos tibiales) y heridas penetrantes de alta energía en los otros tres pacientes. Solo un paciente (17 %) evolucionó con síndrome dolor regional complejo tipo II.
Evaluación del dolor
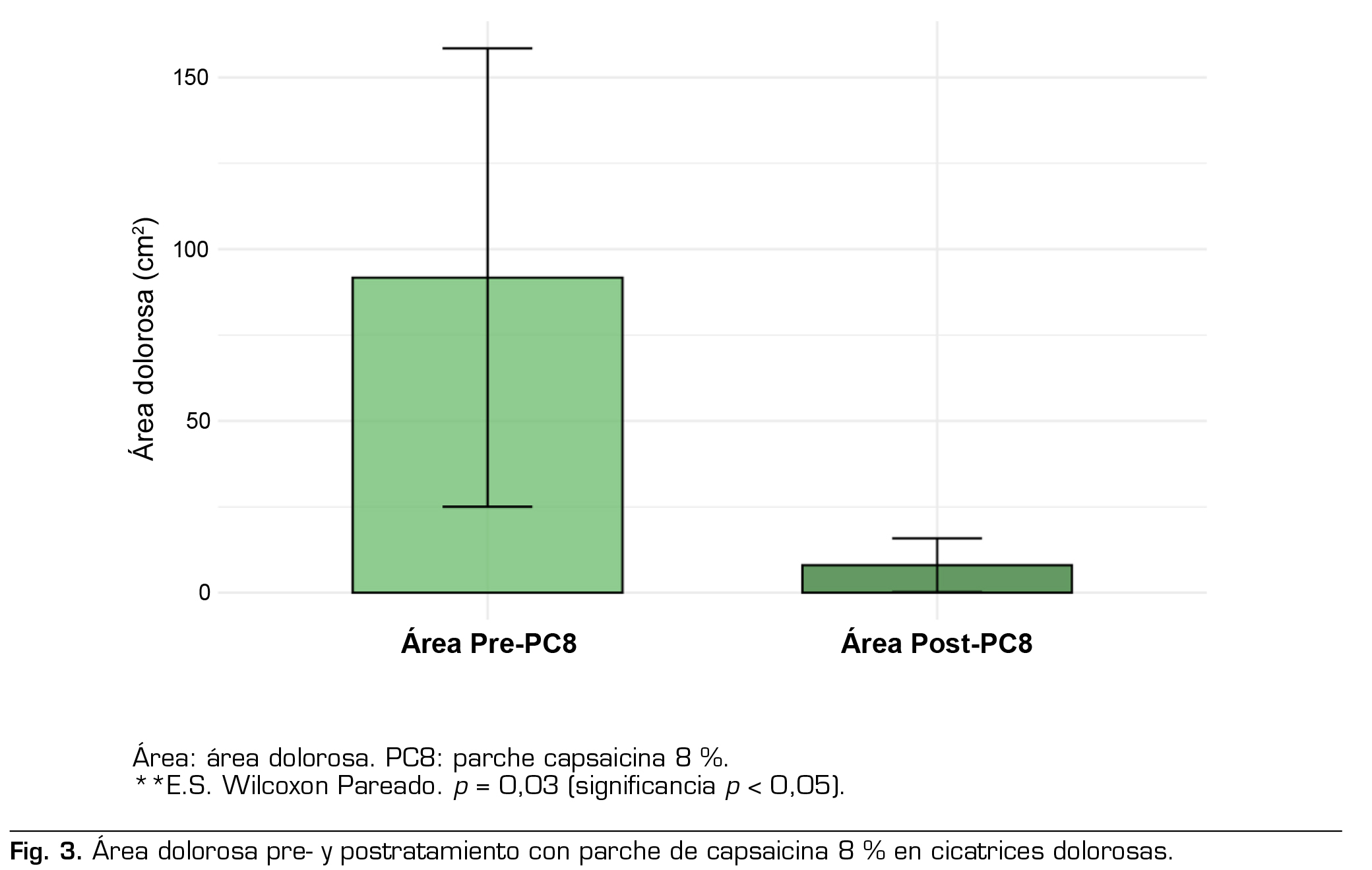
Según la graduación del dolor, tres pacientes presentaron DN “probable” y otros tres pacientes “definitivo”. La intensidad del dolor inicial (NPRS) fue de 7,50 ± 1,48 puntos, cinco pacientes (83 %) tuvieron NPRS ≥ 7. La duración promedio previo al inicio del tratamiento fue 7,2 ± 1,4 años. En la cualidad del dolor (DN4), el puntaje promedio de la población fue de 6,0 ± 1,6 puntos, con todos los pacientes con un puntaje ≥ 3/7. Área dolorosa: el tamaño promedio del área dolorosa al comienzo del estudio fue de 91,7 cm2.
Comorbilidades
En la serie ‘Cicatrices’ se contabilizaron 11 comorbilidades en cinco pacientes, 1,8 patologías por paciente (mediana 1,5; rango 0-5).
Cuatro pacientes presentaron patología psiquiátrica (ansiosa y/o depresiva) derivada del accidente, 2 reportaron antecedentes cardiovasculares (infarto al miocardio e hipertensión arterial), 2 trastornos metabolismo de la glucosa y otros 2 refirieron dolor lumbar degenerativo.
Analgesia concomitante
En la serie ‘Cicatrices’, antes de la aplicación de PC8, se utilizaban 30 analgésicos en los seis pacientes, 5 ± 1,3 analgésicos por paciente (mediana 5; rango 2-7). Al comienzo del estudio, todos los pacientes usaban más de un medicamento analgésico: todos utilizaban opioides potentes (tapentadol) y tres de ellos, además, tramadol de liberación rápida con dosis equivalente a morfina (DEM) promedio de 154,2 ± 15,1 mg/día oral (mediana 160; rango 131-167).
Todos los casos usaban gabapentinoides (pregabalina) en dosis de 325 ± 155 mg/día (mediana 375; rango 75-450). Un paciente usaba duloxetina previo al comienzo del estudio y tres pacientes paracetamol, celecoxib y diclofenaco en gel.
Intervencionismo previo
Todos los pacientes fueron sometidos a técnicas intervencionistas previo a la aplicación de PC8, con un total de 77 procedimientos. Se realizaron promedio de 12,8 ± 8,3 bloqueos por paciente (moda 22, rango 3 a 22 procedimientos). cuatro radiofrecuencias pulsadas perineurales, 37 bloqueos perineurales, 10 bloqueos interfasciales con esteroides, 23 bloqueos de puntos gatillo musculares y tres infiltraciones de la cicatriz dolorosa.
Evaluación del dolor después del tratamiento
Se realizaron 23 aplicaciones de PC8 repartidas en los seis pacientes, en cinco de ellos se realizaron cuatro aplicaciones y, en el paciente restante, tres aplicaciones.
Se hicieron visitas periódicas, con un total de 14,8 ± 2,6 controles en el periodo estudiado. Después de tratamiento promedio de 47 ± 9,1 semanas (mediana 49,4; rango 29,1-53,4), todos los pacientes alcanzaron analgesia estable.
A las 12 semanas se observó disminución de la intensidad del dolor espontáneo (NPRS) de 1,8 ± 1,0 puntos, equivalente a reducción de 26 % de la intensidad del dolor basal y una reducción del área dolorosa de 53,5 % en promedio.
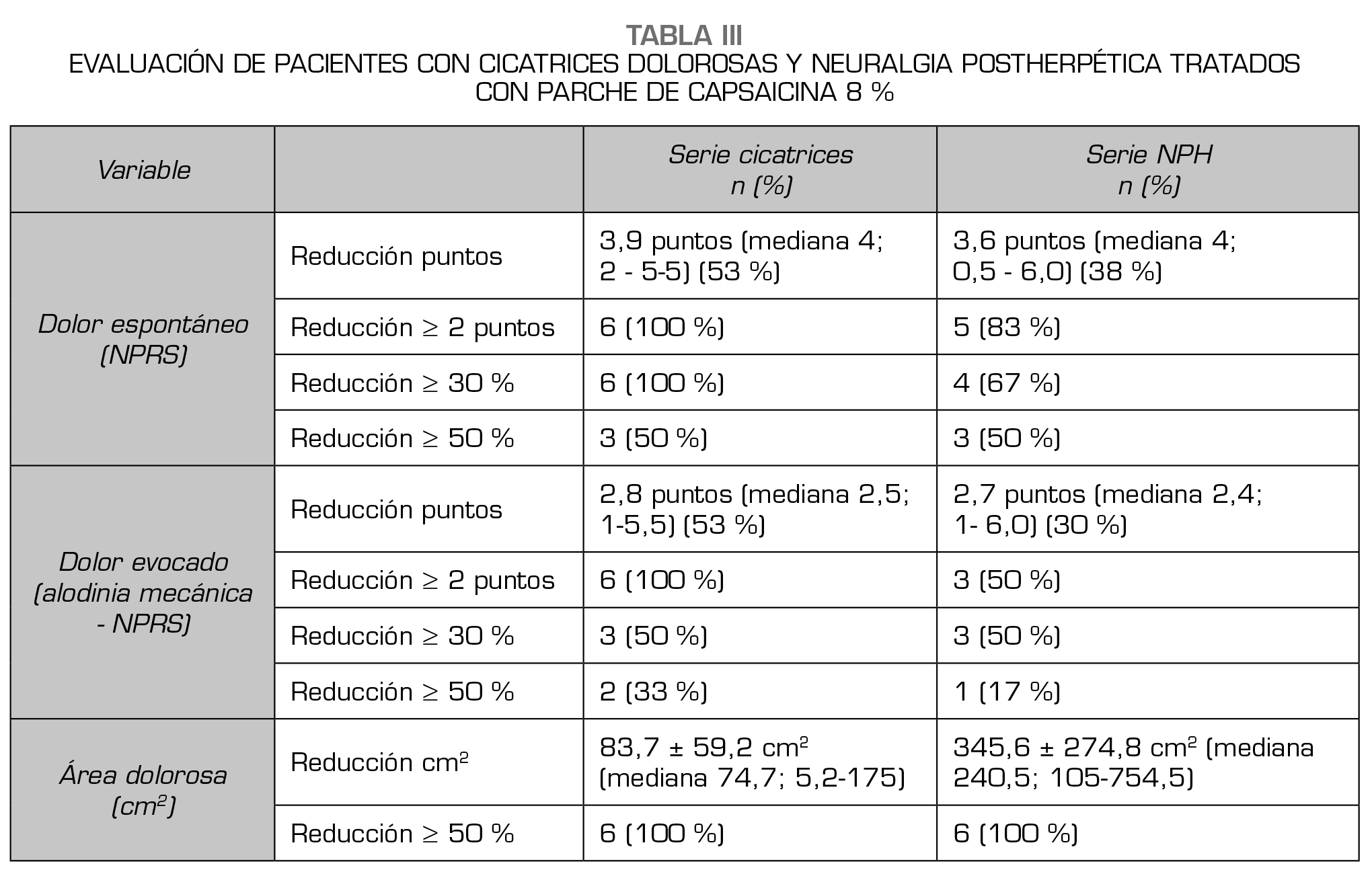
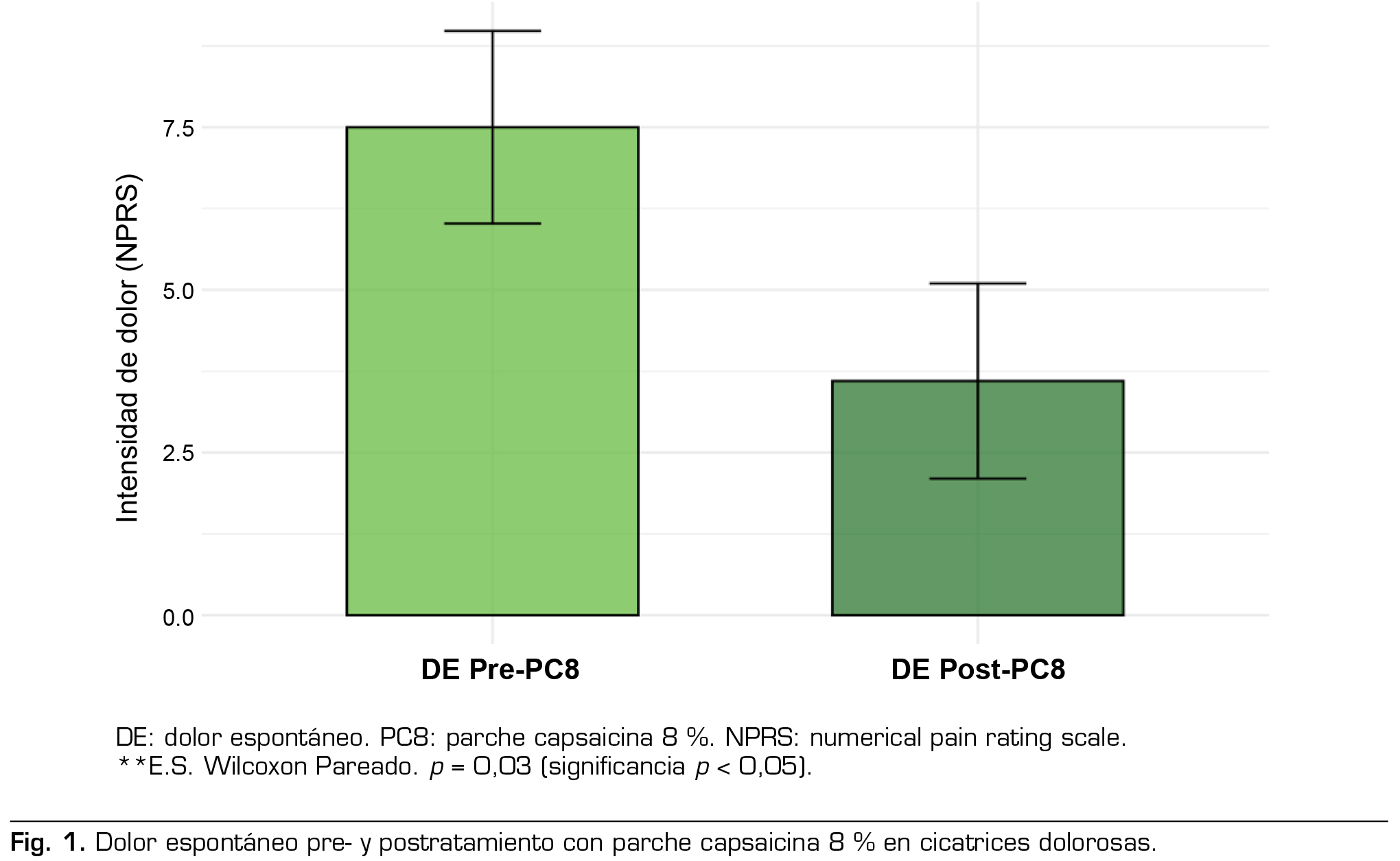
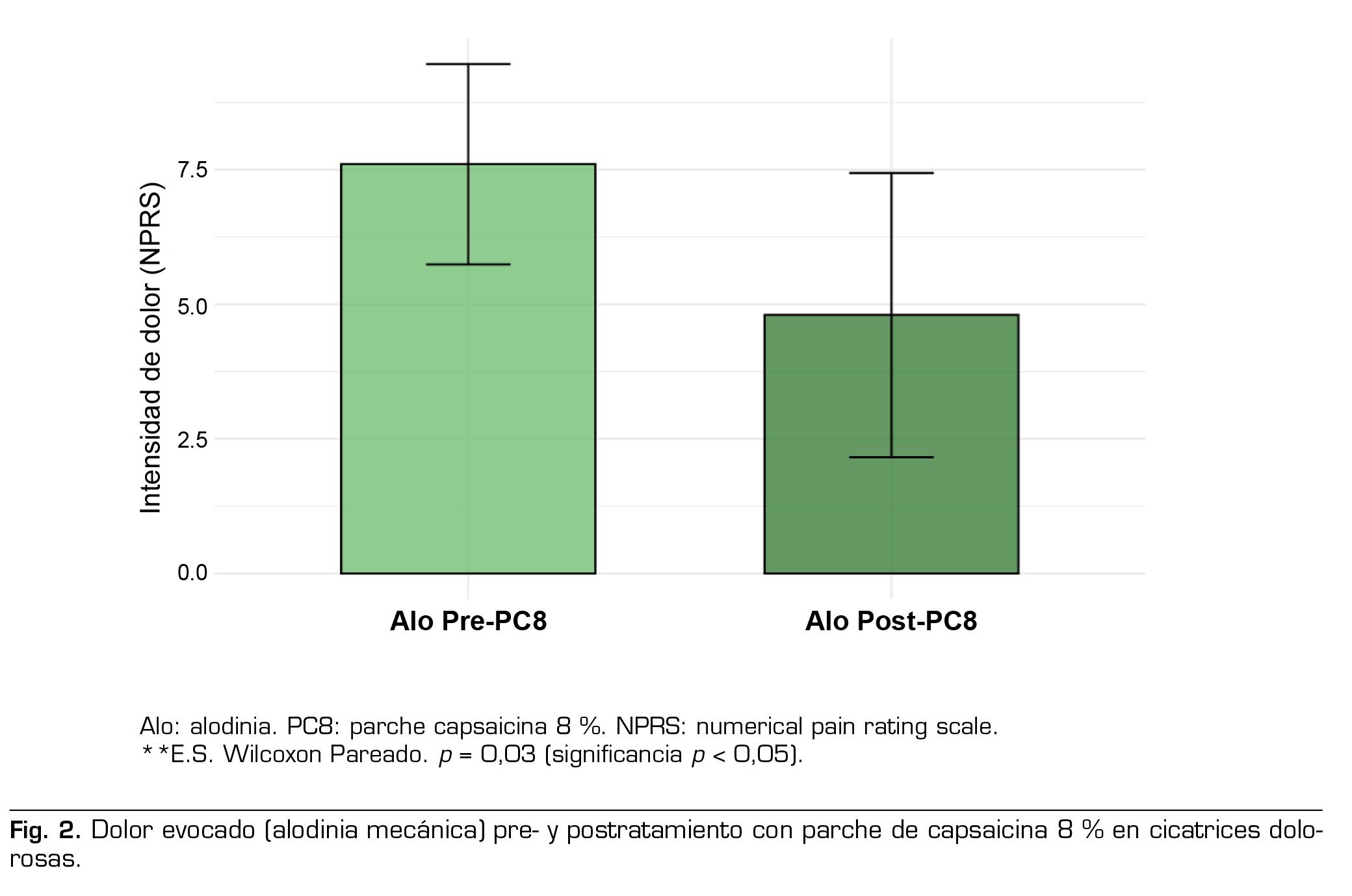
Los resultados finales del tratamiento con PC8 se detallan en la Tabla 3 y Figuras 1, 2 y 3.
No se observó correlación entre puntuación de DN4 inicial y disminución en puntaje de NPRS de dolor espontáneo posterior al tratamiento con PC8 (r= -0,5437).
Calidad de vida
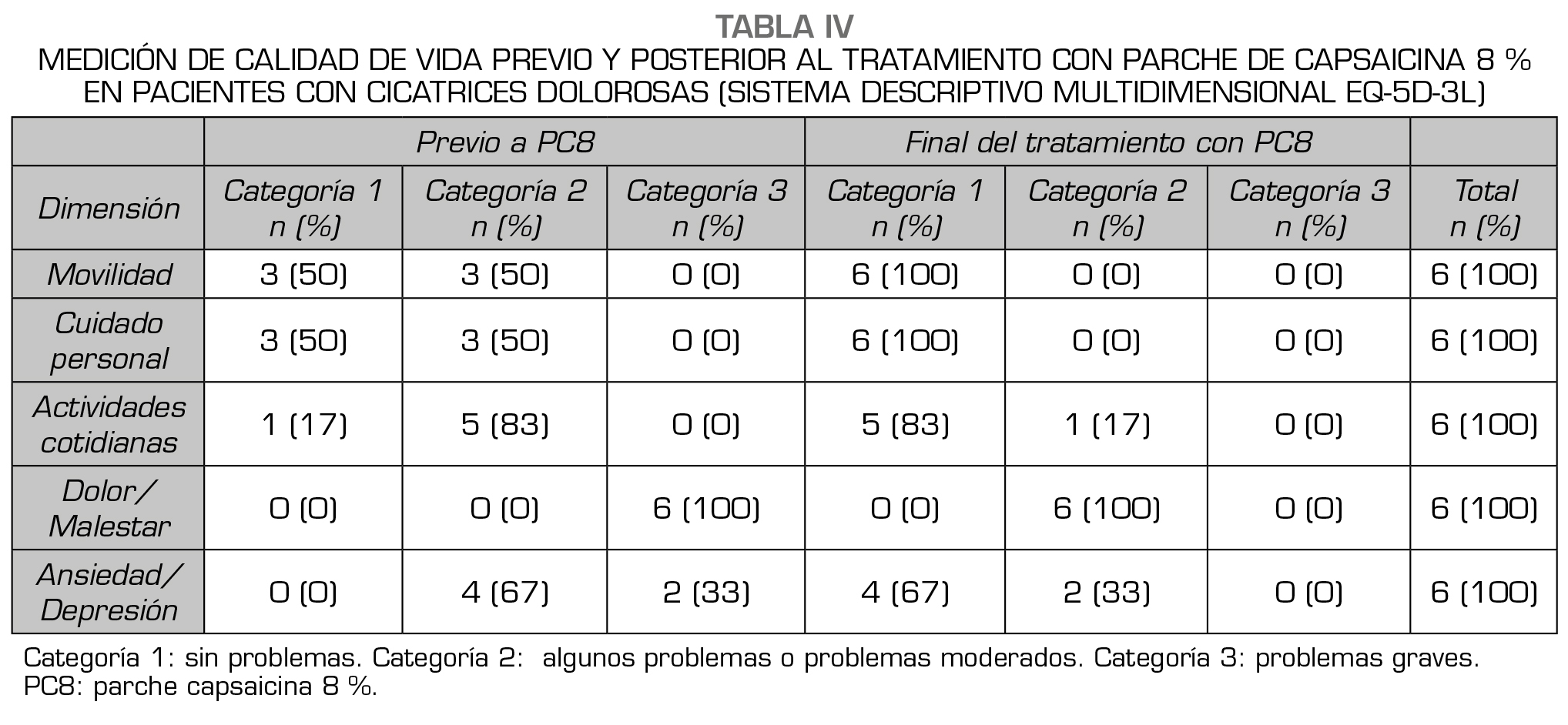
Al evaluar la calidad de vida utilizando el EQ-5D-3L en los pacientes de la serie ‘Cicatrices’ se observó una mejoría de todas las dimensiones al comparar esta serie previo y posterior a las aplicaciones de PC8, siendo más evidente la mejoría de las ‘actividades cotidianas’, seguido por ‘ansiedad /depresión’ y por la ‘movilidad’ y ‘cuidado personal’. El alivio del dolor que se obtuvo en todos los pacientes con PC8 hizo que se desplazaran desde la categoría 3 (‘problemas graves’) a la categoría 2 de ‘algunos problemas o problemas moderados’ (Tabla 4).
Impacto sociolaboral
Antes del accidente que provocó la cicatriz dolorosa, todos los pacientes estaban laboralmente activos. Al comienzo del tratamiento con PC8, solo cuatro pacientes trabajaban (66,7 %), dos no podían a causa del DN. Después de la terapia con PC8, ambos pacientes retornaron al mundo laboral.
Tolerabilidad
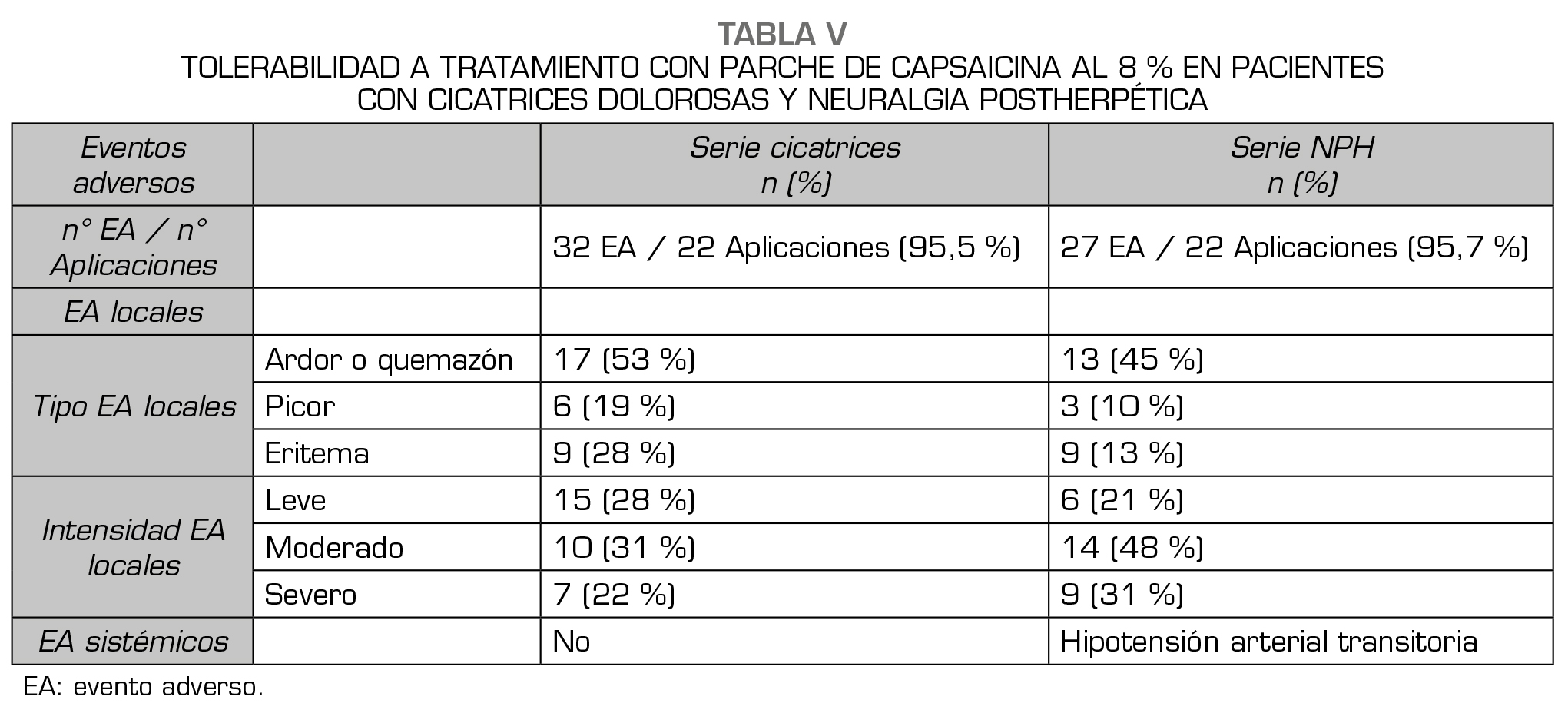
Se observaron 32 eventos adversos durante la administración de PC8 en 22 aplicaciones (95,7 %). El evento adverso más frecuente fue dolor tipo ardor. Los eventos adversos se detallan en la Tabla 5.
En ningún paciente los efectos adversos impidieron la aplicación de PC8 durante el tiempo planificado. Todos los efectos adversos locales mencionados fueron transitorios, con duración máxima de 3 días. No se observaron reacciones adversas tardías con capsaicina 8 % y todos los pacientes consintieron el retratamiento.
Reducción de medicación analgésica
Tras la aplicación de PC8 y al final de este estudio, todos los pacientes de esta serie mantuvieron el uso de opioides con 30,5 ± 18,7 mg/día oral DEM (mediana 27,5; rango 4-40). La reducción de opioides a las 47 semanas de tratamiento alcanzó a 123,7 ± 30,3 mg/día DEM (mediana 128; rango 80-163), equivalente a disminución de 80 % de dosis de opioides respecto del basal.
No se observaron reducciones significativas de dosis de gabapentinoides ni antidepresivos duales con el uso de PC8 en esta serie.
Serie ‘NPH’
Datos demográficos
La población estudiada consistió en 4 mujeres y 2 hombres, con edad promedio de 74,6 ± 22,6 años (rango 33-92).
Evaluación del dolor
Según la graduación del dolor, cuatro pacientes presentaron DN ‘probable’ y otros dos pacientes ‘definitivo’. La intensidad del dolor (NPRS) al comienzo del estudio fue 8,8 ± 1,5 puntos, cinco pacientes (83 %) tuvieron puntajes ≥ 7. La duración promedio previo al inicio del tratamiento fue 2,4 ± 1,9 años. En la cualidad del dolor (DN4), el puntaje promedio de la población fue de 5,2 ± 1,5 puntos, con todos los pacientes con un puntaje > 3/7. Área dolorosa: el tamaño promedio del área dolorosa al comienzo del estudio fue de 356 cm2.
Cinco de seis pacientes de esta serie presentaron DNL, de acuerdo con la herramienta diagnóstica usada. Una paciente (89 años, NPH severa, multi mórbida) tenía área basal de 756 cm2, ligeramente superior a DIN folio A4. Debido a su intenso dolor y ausencia de otras alternativas, se decidió incluirla en el estudio.
Comorbilidades
En la serie ‘NPH´ se contabilizaron 30 comorbilidades en los seis pacientes, 5,0 ± 2,1 patologías por paciente (mediana 5,5; rango 2-7). Dos pacientes presentaron patología psiquiátrica (depresión secundaria a la enfermedad), cuatro de ellos antecedentes cardiovasculares (infarto al miocardio e hipertensión arterial), cuatro con trastornos metabolismo de la glucosa, dos con artrosis severa de rodilla y dos con patología autoinmune que requirió tratamiento inmunosupresor, tras el cual sobrevino NPH.
Analgesia concomitante
En la serie ‘NPH´, antes de la aplicación de PC8, se utilizaban 20 analgésicos en los seis pacientes, 3 ± 1,6 analgésicos por paciente (mediana 3; rango 1-5). Al comienzo del estudio, todos los pacientes usaban más de un medicamento analgésico: tres usaban opioides débiles (tramadol de liberación rápida) DEM promedio de 6,7 ± 12,1 mg/día oral (mediana 2; rango 4-31). Ningún paciente de esta serie usaba opioides potentes. Pregabalina se utilizó en cuatro pacientes, con dosis de 197 ± 187 mg/día (mediana 150; rango 37,5-450). Duloxetina (dosis 40 mg/día, rango 30-60) y paracetamol en tres pacientes. Eslicarbazepina, celecoxib y diclofenaco en gel en un paciente. Todos los pacientes presentaban intolerancia al uso de mayores dosis de medicación debido a efectos secundarios centrales.
Intervencionismo previo
Solo un paciente (17 %) fue sometida a siete técnicas intervencionistas previo a la aplicación de PC8: seis bloqueos perineurales y un bloqueo interfascial tipo ESP, sin resultados positivos.
Evaluación del dolor después del tratamiento
En total, se realizaron 23 aplicaciones de PC8, en cinco pacientes se realizaron cuatro, y en el restante, tres aplicaciones.
Se hicieron visitas periódicas, con un total de 14,2 ± 2,3 controles en el periodo estudiado. Después de tratamiento promedio de 43,5 ± 7,2 semanas (mediana 42,2; rango 34,9-52,7) todos los pacientes alcanzaron analgesia estable.
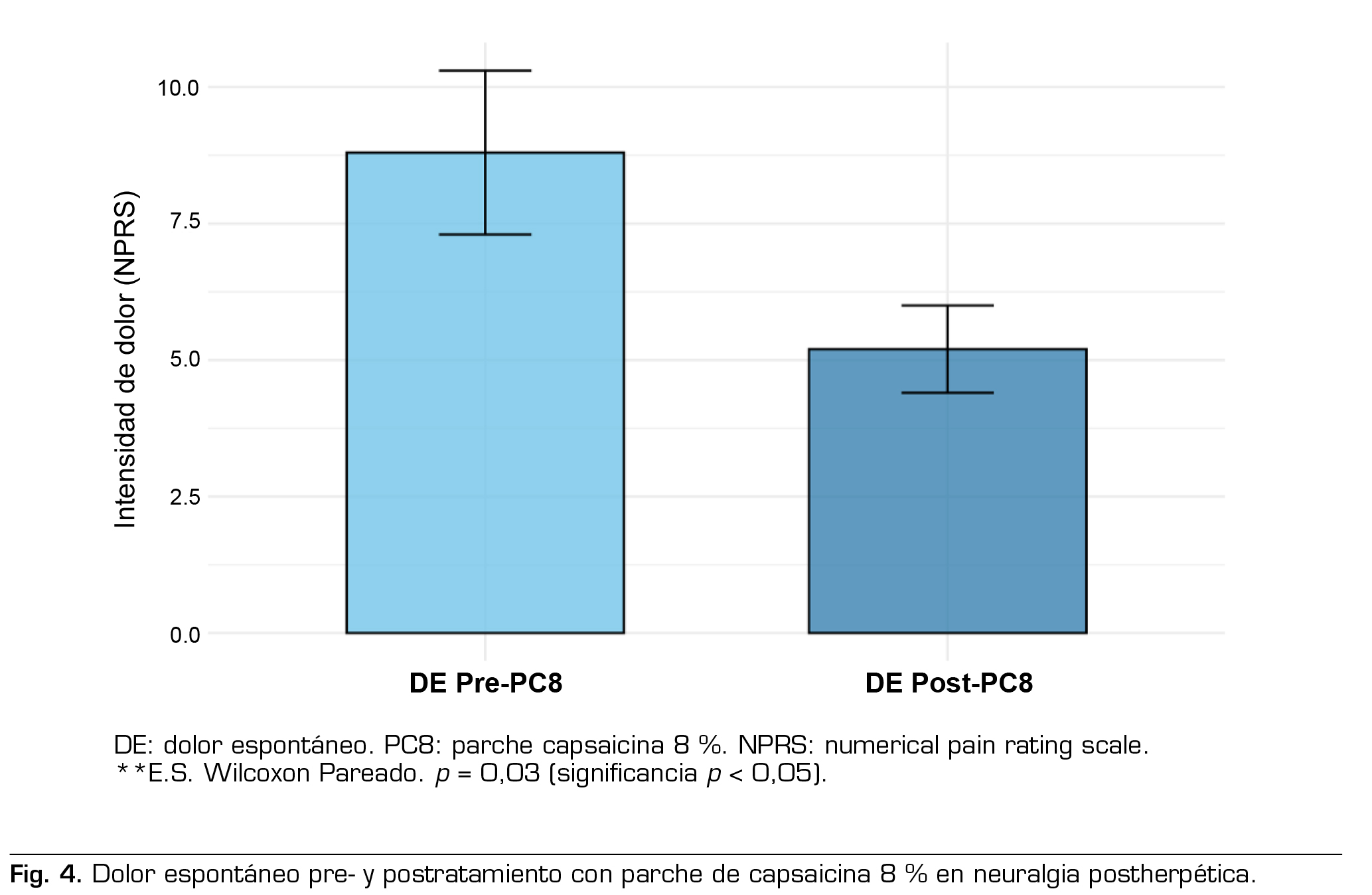
A las 12 semanas se observó disminución de la intensidad del dolor espontáneo (NPRS) de 2,5 ± 1,7 puntos, equivalente a reducción de 28 % de la intensidad del dolor basal y una reducción del área dolorosa de 61,5 % en promedio.
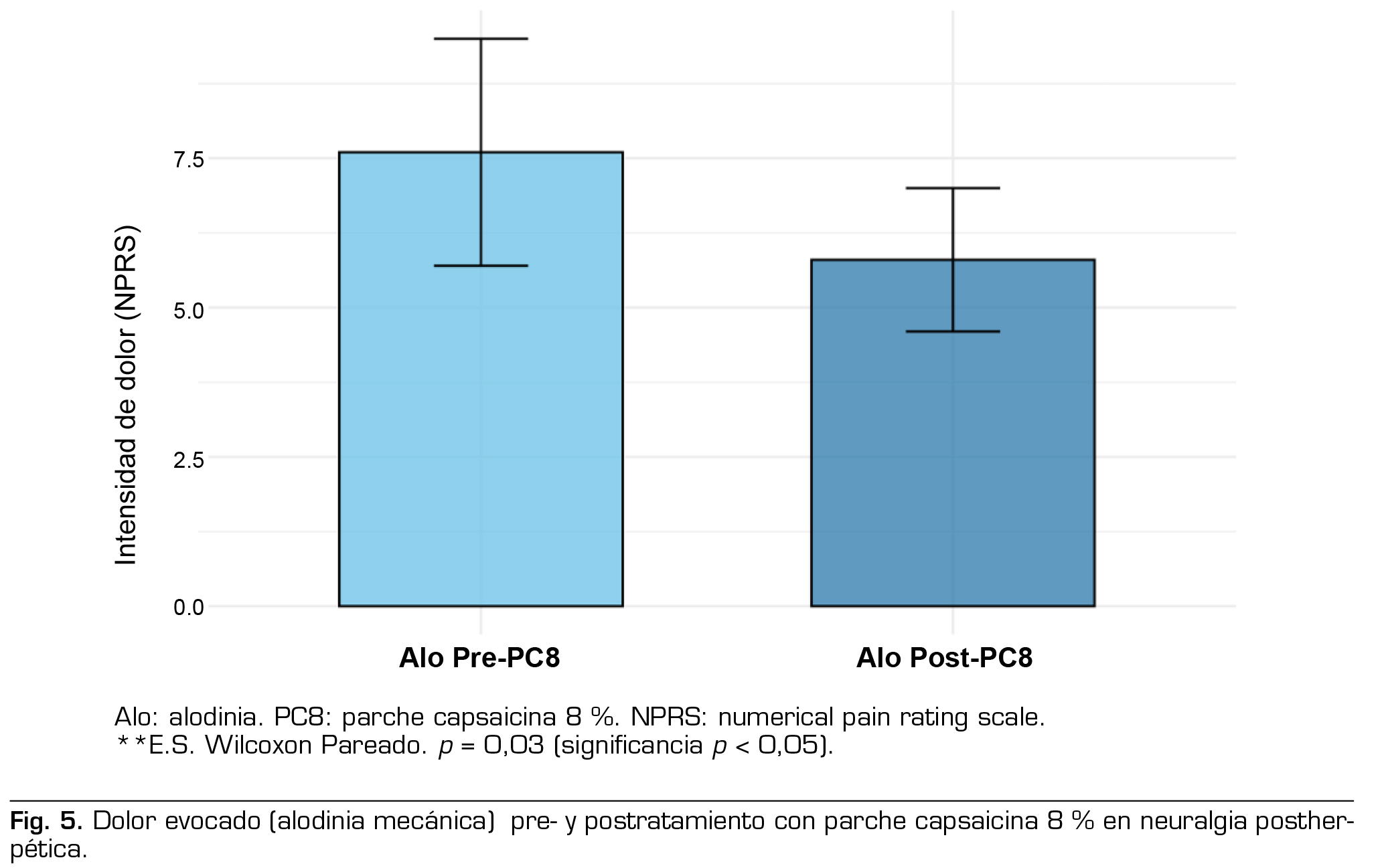
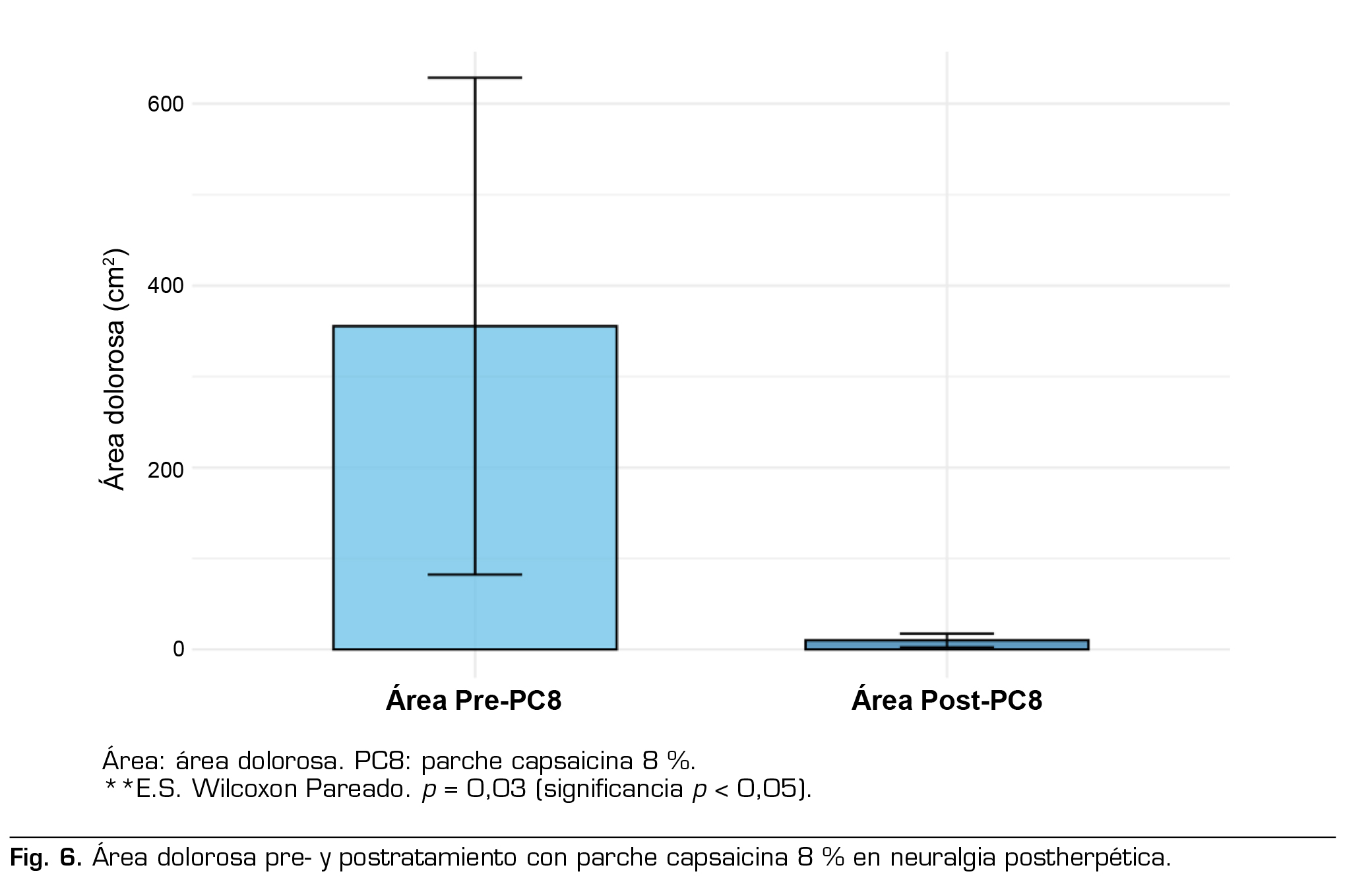
Los resultados del tratamiento con PC8 al final del estudio se detallan en la Tabla 3 y en las Figuras 4, 5 y 6.
No se observó correlación entre puntuación de DN4 inicial y disminución en puntaje de NPRS de dolor espontáneo posterior al tratamiento con PC8 (r = -0.3922).
Calidad de vida
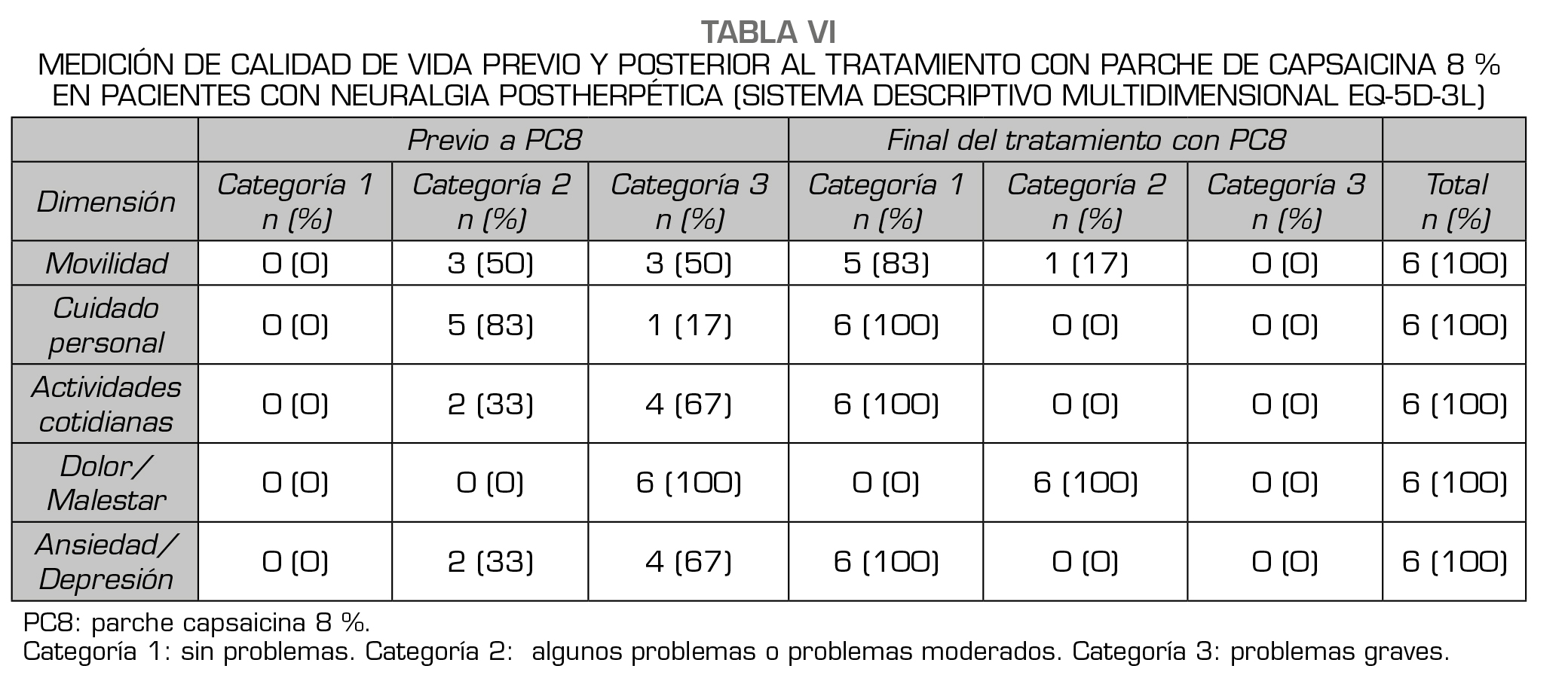
Al evaluar la calidad de vida utilizando EQ-5D-3L en los pacientes de la serie ‘NPH’, se observó una mejoría de todas las dimensiones al comparar esta serie previo y posterior a las aplicaciones de PC8, siendo más evidentes las mejoras en ‘cuidado personal’, ‘actividades cotidianas’ y ‘ansiedad/depresión’, seguido por la ‘movilidad’. El alivio del dolor se obtuvo en todos los pacientes con PC8 e hizo que los seis se desplazaran desde la categoría 3 -’problemas graves’ - a la categoría 2 de ‘algunos problemas o problemas moderados’ (Tabla 6).
Impacto sociolaboral
Cinco pacientes (83 %) de la serie eran mayores y se encontraban retirados del mundo laboral. Sin embargo, antes de presentar NPH todos estaban activos socialmente, en actividades remuneradas o no remuneradas. Un paciente, en edad productiva, trabajaba como profesora de primaria.
Al comienzo del tratamiento con PC8, ninguno de los adultos mayores realizaba actividades y todos estaban aislados socialmente debido al intenso dolor que presentaban. La paciente en edad productiva realizaba su profesión con dificultad y varias restricciones derivadas del dolor que sufría.
Después del tratamiento con PC8, cuatro de los adultos mayores que no realizaban ninguna actividad, lograron retomarlas -1 en servicio remunerado de cuidado de niños después de la escuela, otro en cultivo de hortalizas de su huerto y dos pacientes retomaron sus actividades en el hogar. La paciente en edad productiva, a propósito del alivio del dolor, mejoró su rendimiento profesional, realizó nuevas actividades tanto curriculares como extracurriculares.
Tolerabilidad
Se observaron 27 eventos adversos durante la administración del PC8 en 22 aplicaciones (95,7 %). Los eventos adversos locales fueron los más frecuentes, de ellos el dolor tipo ardor durante la aplicación fue el más prevalente. La intensidad del ardor y picor fue severa en siete aplicaciones (22 %) y el eritema fue moderado a severo en dos tercios de los casos de esta serie. Los eventos adversos se detallan en la Tabla 5.
En una paciente con antecedente de tratamiento inmunosupresor en la que se realizaba su cuarta aplicación de PC8, se observó hipotensión arterial desde 112/65 mmHg (PAM 75) hasta 80/49 (PAM 59). La hipotensión cedió a los pocos minutos de retirado el parche, retornando la tensión a los valores previos (110/69 mmHg [PAM 85]). Cabe destacar que en ninguna de las tres aplicaciones anteriores de PC8 la paciente había presentado baja tensional.
A ningún paciente de la serie se le debió suspender la aplicación del PC8 antes del tiempo predeterminado debido a la presencia de efectos adversos durante el procedimiento. Todos los efectos adversos mencionados, locales y sistémicos, fueron transitorios, con duración máxima de tres días. No se observaron reacciones adversas tardías con PC8. Ninguno de los efectos adversos condicionó su aplicación posterior, consintiendo todos los pacientes el retratamiento con PC8.
Reducción de medicación analgésica
Tras las aplicaciones de PC8 y al final del estudio, dos pacientes mantenían el uso de opioides con promedio de 1,9 ± 4,0 mg/día oral DEM (rango 1,4-10). La reducción de opioides a las 43,5 semanas alcanzó a 4,8 ± 8,2 mg/día DEM (mediana 2; rango 4-21), equivalente a disminución de 40 % de la dosis de opioides inicial.
No se observaron reducciones significativas de dosis de gabapentinoides con el uso de PC8 en esta serie. Respecto de los antidepresivos duales, con el tratamiento de PC8 2 pacientes suspendieron su uso y otro mantuvo una dosis de 30 mg/día.
DISCUSIÓN
Consideramos que la clave para obtener una respuesta adecuada al tratamiento con PC8 es seleccionar cuidadosamente a la población con dolor neuropático que podría ser candidata al procedimiento, eligiendo solo pacientes con DN probable o definitivo, como fue realizado en esta investigación, utilizando el DN4 y seleccionando exclusivamente pacientes con puntaje ≥ 3/7, alodinia mecánica y ausencia de hipoestesia, eligiendo pacientes con perfil sensitivo de ‘nociceptor irritable’, por la mejor respuesta que este perfil tiene ante la aplicación de PC8 (26,27).
Al analizar la bibliografía, encontramos estudios con diferentes criterios de selección de pacientes, en un estudio abierto aleatorizado (22) se hace referencia a que 55 % pacientes tenían DN probable y 45 % definitivo, obteniendo resultados similares de efectividad respecto de la intensidad del dolor a los obtenidos en nuestro estudio. Esto contrasta con la mayoría de los estudios, donde no se describe una sistematización rigurosa para la confirmación de presencia de dolor neuropático. En un estudio que aplicó el Cuestionario Pain Detect (PDQ) en 1008 pacientes tratados con PC8 (28), el 18 % de ellos tenían puntajes negativos para dolor neuropático, el 8 % presentaba hipoalgesia y el 17 % hipoestesia térmica, no correspondiendo al perfil de “nociceptor irritable”. Cabe destacar que en este estudio el 23 % de esos pacientes no redujo la intensidad del dolor con el uso de PC8.
Asimismo, se debería hacer énfasis en la búsqueda activa y priorizar aquellos con DN Localizado con áreas dolorosas con alodinia mecánica bien definida.
En todos los pacientes de ambas series del estudio se realizaron al menos tres aplicaciones y en 10 de los 12 pacientes (83 %) se realizó una cuarta aplicación de PC8, observándose un efecto acumulativo evidenciable en el aumento de respuesta en relación al área y la intensidad del dolor con cada aplicación subsecuente, esto se condice con la literatura, donde un estudio muestra una tendencia clara de mejoría de respuesta conforme se realizan aplicaciones sucesivas (29).
El intervalo entre aplicaciones utilizado fue de tres meses entre procedimientos, a excepción de tres casos, donde el intervalo se redujo a dos meses, en consideración a la intensidad del dolor y respuesta a la aplicación previa de cada caso, utilizando los intervalos recomendados por la EMA (11).
Se ha observado que, aunque este tratamiento influye tanto en el área como en la intensidad del dolor espontáneo, estas dos variables no estarían correlacionadas entre sí (30). De hecho, en la investigación del autor, dos pacientes de la serie ‘NPH’ no tuvieron reducción del dolor espontáneo clínicamente relevante (< 30 %), sin embargo, en ambos casos se observó una reducción del área dolorosa superior al 30 %. Estas observaciones son similares a la reportadas por otros autores (31,32) donde los pacientes ‘no respondedores’ (reducción dolor espontáneo < 30 %), redujeron ≥ 30 % su área dolorosa a los 90 días o en la ‘última aplicación’ de PC8.
Observamos que la disminución del dolor espontáneo a las 12 semanas fue similar porcentualmente en ambas series (el 26 % en serie “Cicatrices” y el 28 % en serie “NPH”). Nuestros hallazgos son similares a la literatura, donde estudios con pacientes con NPH reportaron reducción del dolor entre 20 y 32 % (8,23,33) y, otros estudios (5,34) que analizaron múltiples patologías dolorosas no diabéticas, con claro predominio de NPH y dolor postraumático y postquirúrgico, la disminución de la intensidad del dolor espontáneo fluctuó entre 27 % y 37 % a los tres meses de la aplicación de PC8. En nuestro estudio, al final del seguimiento, todos los pacientes de la serie ‘Cicatrices’ y ? de la serie ‘NPH’ redujeron en ≥ 30 % la intensidad de dolor basal y en ambas series del estudio la mitad de los pacientes redujeron ≥ 50 % la intensidad del dolor espontáneo. Los resultados de nuestro estudio serían mejores a los estudios a largo plazo encontrados, donde uno de ellos (34) que realizó esta medición en ambas patologías, observó que la mitad de los pacientes disminuían ≥ 30 % su dolor basal y casi ? de ellos ≥ 50% tras la tercera aplicación de PC8.
A los tres meses de la primera aplicación de PC8, el área dolorosa disminuyó en ambas series del estudio de forma similar en términos porcentuales (54 % en serie ‘Cicatrices’ y 62 % en serie ‘NPH’), lo cual es superior a un estudio retrospectivo revisado (35), en el cual se observó que el área dolorosa se redujo en 42 % y 35 %, respectivamente. Asimismo, al final del estudio, todos nuestros pacientes de ambas series redujeron su área dolorosa 90 % o más. En un estudio prospectivo (36) se observó reducción del área dolorosa en el 47 % de los pacientes con dolor postquirúrgico tras su tercera aplicación de PC8. En un estudio retrospectivo (32) realizado solo en pacientes con NPH y dolor postraumático postquirúrgico, se observó una reducción del área dolorosa de 23 % para NPH y de 35 a 41 % para dolor postraumático/postquirúrgico, desde el inicio del tratamiento hasta el ‘último tratamiento’, tras la segunda o tercera aplicación de PC8. En otro estudio retrospectivo (30) mayoritariamente de NPH y dolor postraumático y postquirúrgico se observó una reducción del 50 % del área dolorosa en ambas patologías desde el nivel basal hasta el ‘último tratamiento’. Impresiona que la disminución del área dolorosa con uso de PC8, no se haya cuantificado en la mayoría de los estudios, siendo que se considera una variable de respuesta al tratamiento tópico (≥ 30 % de reducción del área dolorosa), según el consenso realizado en 2016 (25). Esto es relevante desde el punto de vista funcional, especialmente cuando se observa compromiso doloroso de extremidades, afectando significativamente la calidad de vida.
La disminución de la alodinia mecánica en la zona dolorosa se registró en todos los pacientes de ambas series y se observó una reducción al final del estudio de aproximadamente un tercio de la intensidad del dolor evocado basal (38 % para serie ‘Cicatrices’ y 30 % para serie ‘NPH’), y en ambas series en la mitad de los pacientes se redujo la intensidad de la alodinia mecánica ≥ 30 % del nivel basal. En la literatura se encontraron escasos reportes de la disminución de este aspecto del dolor neuropático, en un estudio abierto (28) a los 3 meses se observó reducción o desaparición de la alodinia mecánica en 44 % de los casos y en el otro (5) a las 52 semanas se reportó disminución de la alodinia mecánica en el 18 % de los pacientes. Un estudio retrospectivo (32) menciona reducción de la alodinia mecánica del 54 % en NPH y del 66 % en dolor postquirúrgico, desde la primera hasta el ‘último tratamiento’, con gran dispersión de aplicaciones de PC8 realizadas en ese estudio (2 a 12).
Todos los pacientes de ambas series utilizaron opioides, lo que podría interpretarse a la luz de la refractariedad y cronicidad del dolor. En la serie ‘Cicatrices’ es especialmente frecuente el uso de opioides potentes (tapentadol) en dosis altas, en contraste con la serie ‘NPH’ donde solo la mitad de los pacientes utilizó opioides débiles y en dosis 20 veces más baja, debido a problemas de tolerabilidad y riesgo de caídas. Como resultado del uso de PC8, se destaca la reducción del tratamiento opioide oral, especialmente en la serie ‘Cicatrices’ donde la disminución alcanzó al 80 % de la dosis basal, el doble de la reducción de opiáceos obtenida en la serie ‘NPH’.
Se utilizó pregabalina en dos tercios de los pacientes de la serie ‘NPH’ y en todos los de la serie ‘Cicatrices’. La dosis fue aproximadamente el doble en la serie ‘Cicatrices’, usándose además como ansiolítico e hipnótico. Posterior a las aplicaciones de PC8, no se observaron reducciones significativas del uso de gabapentinoides en la serie ‘Cicatrices’, probablemente debido a la patología psiquiátrica prevalente en ella. En la serie ‘NPH’, tampoco se observó disminución del uso de gabapentinoides, aunque en este caso, se puede atribuir a la dosis baja del medicamento y su uso como coadyuvante.
La evidencia es inconsistente respecto a la disminución del uso de analgesia concomitante, un autor (28) expresa disminuciones globales del 63 % al 74 % del uso de analgésicos, y otra, en cambio, en un estudio retrospectivo de más reciente publicación (35), muestra una reducción del 21 % del uso de analgésicos en NPH y del 16 % en dolor postquirúrgico.
En las dimensiones de calidad de vida evaluadas por EQ-5D-3L se observó una mejoría en todas ellas en nuestro estudio, particularmente en las de ‘actividades cotidianas’ y ‘ansiedad/depresión’ en ambas series de pacientes. El alivio significativo del dolor se observó en todos los pacientes de ambas series, desplazando su categorización desde ‘problemas graves’ a ‘algunos problemas o problemas moderados’. En la literatura se describe la aplicación de distintos cuestionarios de evaluación de calidad de vida según el estudio, como EuroQoL (5,22,34,37,38), SF-36 (8,23), SF-12 (28,39), sin embargo se menciona muy escuetamente los beneficios en calidad de vida que reporta este tratamiento. Destaca un estudio abierto, de práctica clínica, a largo plazo con múltiples aplicaciones de PC8 en diferentes patologías dolorosas (34) donde se reporta que el medicamento tópico habría duplicado la calidad de vida en los pacientes tratados.
La condición social y laboral de los pacientes es un aspecto importante a considerar, según lo descrito por la última guía alemana de DN (24) donde se consideran dentro de los objetivos terapéuticos realistas a lograr en su tratamiento.
En nuestro estudio destaca que en ambas series se evidenció una mejora en este aspecto, retornando 11/12 pacientes (92 %) al mundo laboral y/o actividades del hogar. Solo un paciente, mayor, multimórbido, portador de NPH, que a pesar de obtener mejoría del dolor con PC8, mantiene un estado ansioso depresivo de difícil tratamiento, con respuesta parcial a la medicación y no ha logrado aún reinsertarse ni social ni laboralmente. De los estudios realizados a la fecha, destaca un estudio prospectivo, no intervencional (28) en el cual se señala que el 30 % de los pacientes volvieron a realizar las actividades cotidianas que no podían realizar por dolor.
La terapia con PC8 fue, en términos generales, bien tolerada en nuestro estudio. Sin embargo, se reportaron con alta frecuencia la presencia de eventos adversos (EA) locales en ambas series, ascendiendo a 22 de las 23 aplicaciones (95,7 %) de cada casuística. El EA más frecuente en ambas series fue el dolor tipo ardor. En la literatura la mención sobre EA es variada, con predominio de presentación de eventos adversos locales entre el 60 y 99 % de las aplicaciones realizadas (5,8,22,23,40,41). En todos los estudios, los EA más frecuentes fueron el dolor tipo ardor y el eritema. Se reportaron EA serios entre el 4 a 13 % de las aplicaciones (5,8,22,23,33,41).
Todos los EA se produjeron durante las aplicaciones de PC8 y fueron transitorios. En ninguna de las aplicaciones se debió retirar el fármaco tópico antes del tiempo programado por la presencia de EA durante el procedimiento. Asimismo, en la literatura se observa que el retiro prematuro del tratamiento tópico por EA se presenta con baja frecuencia, 0,5 % a 3,6 % de los casos (5,8,23,33). Ninguno de los EA condicionó la aplicación posterior, consintiendo todos los pacientes de ambas series el retratamiento con PC8. En la investigación, la edad de los pacientes de la serie ‘NPH’ es mayor por más de 20 años en promedio a la de la serie ‘Cicatrices’, estos años de diferencia pueden asociarse, entre otros, a condiciones cutáneas más desfavorables, con piel más delgada y vulnerable que lleven consigo eventos adversos más severos. Al analizar la intensidad del eritema en nuestra investigación, observamos que en la serie ‘Cicatrices’ en las 9 aplicaciones que cursaron con eritema, esta fue de intensidad leve, mientras que en la serie ‘NPH’ donde se presentó el mismo número de casos con eritema, la intensidad fue moderada a severa en dos tercios de las aplicaciones. Asimismo, en un análisis agrupado reciente, que comparó pacientes ≥ 75 años con pacientes menores (41), el eritema es significativamente más frecuente en el grupo de adultos mayores que en los más jóvenes (≥ 75 años: 42,3 % vs. 25,3 % en < 75 años, Chi2 6,38 p < 0,01). Estos hallazgos apuntan a la mayor fragilidad de la piel del adulto mayor y a la necesidad de mayor supervisión y prevención al momento de la aplicación de PC8 en este grupo etario.
En la revisión sistemática y metanálisis de 229 estudios (42) ubica al tratamiento con capsaicina al 8 % como un fármaco de segunda línea, con una recomendación débil para su uso. Más recientemente, las guías alemana y francesa (24,43) mantienen esta ubicación en el tratamiento del dolor neuropático. La guía francesa destaca además que en los estudios clínicos no es posible garantizar el ciego del paciente por las frecuentes reacciones cutáneas que ocurren con capsaicina, manteniendo una recomendación débil para el uso de PC8 y ubicándola al mismo nivel de la toxina botulínica-A para el tratamiento de DNL. Por su parte, la última revisión Cochrane de 2017 (44) hace observaciones similares y mantiene el nivel mencionado previamente, puntualizando que en las revisiones de 2019 y 2021 no hay ensayos clínicos que hagan cambiar su condición.
Sin embargo, en poblaciones especiales de pacientes como adultos mayores, multimórbidos y/o polimedicados, se ha considerado recomendar, por consenso de expertos y algunas guías, al PC8 como primera línea en DNL, incluidos la NPH y el dolor postraumático/postquirúrgico (10,12).
Aportes del estudio
Esta es la primera experiencia documentada en Latinoamérica del uso de PC8 en pacientes con DN, cumpliendo a plenitud con la norma europea (11). Corresponden a dos series homogéneas de pacientes, portadores de las patologías más prevalentes de DN periférico no diabético, ambas con el mismo perfil sensitivo, incluyendo solo casos crónicos y refractarios a otras terapias y aplicando la misma metodología de evaluación, donde se realizaron de manera seriada tres o cuatro aplicaciones de PC8. Se incluye la medición del área dolorosa en forma sistemática, que sería una de las variables que más disminuiría tras el tratamiento con PC8 y que tendría mayor repercusión en funcionalidad, calidad de vida y aspectos sociolaborales. Se incluye adicionalmente la medición de la intensidad de la alodinia mecánica y su reducción en el tiempo con el tratamiento, siendo este aspecto también relevante en la vida diaria. Ambas variables son poco mencionadas y analizadas en la literatura y estimamos que son elementos relevantes a tener en cuenta para evaluar el resultado de esta terapia.
Limitaciones del estudio
La condición de estudio observacional, retrospectivo, descriptivo, propenso a sesgos de selección e inadecuado control de los factores confundentes, sin comparador activo ni ciego, donde los pacientes saben que se les aplica PC8 y sus efectos analgésicos, sumado a muestras de tamaño pequeño en las series de casos, no permiten sacar conclusiones directas o recomendaciones derivadas de estos datos, sino más bien sugerir tendencias y proponerse como base a estudios posteriores, prospectivos y de mayor tamaño muestral para evaluar nuevas hipótesis.
CONCLUSIONES
El tratamiento con parche de capsaicina al 8 % de cicatrices dolorosas y neuralgia postherpética asociados con dolor neuropático periférico crónico localizado se ha visto que es efectivo en el corto y largo plazo, tanto en disminuir la intensidad del dolor espontáneo y evocado como reducir el área dolorosa, así como el consumo de analgésicos, especialmente opioides, mejorando la calidad de vida y reinserción sociolaboral de los pacientes. Al ser una terapia tópica tiene ventajas en relación con el riesgo de efectos adversos e interacción medicamentosa, representando una importante opción terapéutica en población de riesgo como los adultos mayores, pacientes multimórbidos y/o polimedicados. A pesar del malestar local que induce en la mayoría de los pacientes el PC8 durante o inmediatamente después de su aplicación, el tratamiento es bien tolerado por la mayoría de los pacientes, permitiendo su uso repetido y evidenciando efecto acumulativo. Se requiere administración intrahospitalaria del PC8, bajo directa supervisión médica y tener protocolo de actuación en caso de presentarse EA. Se sugiere que, utilizando la metodología aplicada en esta investigación, se realice un estudio prospectivo, con mayor tamaño muestral, particularmente en pacientes con cicatrices dolorosas con componente neuropático, para evaluar la eficacia y seguridad a largo plazo de PC8 en esta población.
AGRADECIMIENTOS
Agradezco a la Clínica RedSalud Providencia, al Director Médico Dr. Carlos Escobedo y a la Enfermera Jefa Stefany Barrios por su apoyo en esta iniciativa, a mi equipo de trabajo en especial al estudiante universitario sr. Antonio Correa-Torres, que colaboró activamente en la aplicación de los parches de capsaicina al 8 %. Deseo agradecer igualmente, al Hospital Clínico Mutual de Seguridad CChC, en especial a mi jefatura, Dr. Fernando Cubillos y a los Técnicos en Enfermería Angela Yáñez y Víctor Lobos.
Los PC8 usados en este estudio fueron proveídos por Laboratorio Grünenthal Chilena.
CONFLICTOS DE INTERESES
El autor principal informa que al momento de realización del presente estudio no tiene relación personal o financiera con personas u organizaciones que pudieran influenciar inadecuadamente este trabajo. El autor prestó servicios de testimonio de experto remunerado hasta hace 3 años con el laboratorio Grünenthal, productor del fármaco utilizado en este estudio. Actualmente el autor no tiene ninguna relación comercial ni ha recibido ayudas económicas en forma de becas, premios o asesorías del laboratorio mencionado ni de otra institución relacionada.
La presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
BIBLIOGRAFÍA